
Une bouteille de verre coloré.

Bouteille en verre utilisée pour le vin.
On peut distinguer deux définitions du « verre ». La première est la définition au sens commun : le verre est un matériau ou un alliage dur, fragile (cassant) et transparent à la lumière visible, à base d’oxyde de silicium (silice SiO2, le constituant principal du sable) et de fondants: c'est le cas du verre sodocalcique utilisé pour les vitrages. Cette définition commune était la définition aussi adoptée par la communauté scientifique, il y a encore un siècle. Cela est assez logique, puisqu'il y a encore un peu plus d'un siècle, les verres silicatés étaient pratiquement les seuls matériaux transparents que l'on savait produire industriellement. Les verres les plus produits actuellement restant des verres silicatés transparents (fenêtres, vaisselles, verrerie de laboratoire) cette définition persiste.
Extension du mot verre
Le développement de nouveaux matériaux transparents, depuis un siècle, a rendu cette définition désuète et source de confusion (particulièrement parce qu'il est difficile de s'assurer qu'un matériau fragile et transparent est bien d'une part réellement dur et d'autre part réellement fait de silice). L'exemple le plus flagrant est le verre de lunettes, qui bien que l'on les appelle « verre » ne répondent pas à la définition première du verre. Ils ne sont ni particulièrement dur, ni à base de silice (ce sont des matériaux organiques).
On parle également de « perles de verres », pour des matériaux produits depuis plus de 3 000 ans même si ces perles ne sont pas du tout transparentes (l'aspect vitreux suffit à leur attribuer le nom de verre). La laine de verre n'a aucune nécessité d'être transparente, elle peut donc être juste translucide, voire noire (de même pour la mousse de verre). On nomme donc « verre » dans le langage courant des objets qui n'en sont pas faits, au sens de la définition commune du verre. À l'inverse, certains matériaux correspondent parfaitement à la définition commune du verre sans en être : le quartz cristallin ou certaines céramiques sont des matériaux silicatés, durs, fragiles, transparents dans le visible mais ce ne sont pas des verres.
La communauté scientifique donne une autre définition du verre : du point de vue physique, le verre est un matériau amorphe (c’est-à-dire non cristallin) présentant le phénomène de transition vitreuse. En dessous de sa température de transition vitreuse, qui varie fortement avec la composition du verre (plus de 1 000 °C pour la silice vitreuse, moins de 40 °C pour le sélénium amorphe), le verre se présente à l’état vitreux. Aujourd'hui, un grand nombre de solides amorphes sont regroupés sous le nom de « verre ». Ainsi, on fabrique non seulement des verres minéraux, mais aussi des verres organiques et même des verres métalliques.
Types de verres
Il y a un peu plus d'un siècle, n'étaient considérés comme "verre", même pour la communauté scientifique, qu'un matériau ou un alliage dur, fragile (cassant) et transparent à la lumière visible (bien souvent même qu'un alliage à base de silice). À cette époque, le verre était le plus souvent constitué d’oxyde de silicium (silice SiO2, le constituant principal du sable) et de fondants. Dans le langage courant, cette définition persiste, car aujourd'hui encore, parmi tous les types de verre artificiels, le plus courant est le verre sodocalcique.
Il y a plus de quatre mille ans, les céramistes et chaufourniers égyptiens ont découvert qu'en chauffant de la silice SiO2(sable), avec du natron, transformé en soude par dessèchement et purification, et de la chaux vive, ils fabriquaient une matière plus ou moins vitreuse et transparente. En ajoutant certains ingrédients ou poudres minérales colorées au mélange, ces premiers verriers obtenaient des verres spécifiques ou diversement colorés. Les proportions massiques du mélange de départ pour obtenir un verre stable à 650 °C sont d'environ :
SiO2 70 % ;
Na2O équivalent soude 1 % ;
addition nécessaire de fondants : par exemple CaO 10 % et oxydes métalliques divers 5 %.
D'où l'esquisse sans stœchiométrie de la réaction chimique expliquant la formation concrète de matière vitreuse :
-
SiO2solide + Na2CO3solide + ... -→ SiO2.Na2O...verre stable + CO2 gaz
Depuis les années 1920, on a constaté et mis en évidence, par la diffraction des rayons X, qu'une des spécificités des verres étaient leur absence de structure cristalline ("d'ordre") détectable par cristallographie aux rayons X. Cette spécificité n'étant pas propre aux oxydes transparents, mais à tous les amorphes, on a, depuis les années 1920, rassemblé sous le terme "verre" la plupart des solides amorphes. Depuis le début du XX siècle, nombre de définitions ont permis d'élargir la définition désuète du verre (à travers leurs points communs: absence d'ordre, transition vitreuse...) qui le limitait aux matériaux transparents à base d'oxydes. Ainsi, on fabrique non seulement des verres minéraux, mais aussi des verres organiques et même des verres métalliques. On peut regrouper les verres inorganiques sous différentes classes :
verres sodocalciques ;
verres au plomb ;
verres borosilicatés ;
verres oxyazotés ;
verres d'alumino-silicates ;
verres de fluorures ;
verres de phosphates ;
verres de chalcogénures ;
verres métalliques
verre de quartz.
La liste est exhaustive. Parmi ces verres, nombres ne sont pas transparents (verres oxyazotés, verres métalliques…) ou du moins pas dans le visible (verres de chalcogénures). Il est par ailleurs aisé, sans avoir à rajouter des fractions volumiques importantes d'oxydes métalliques, de produire des verres silicatés faiblement transparents voire opaque. L'obsidienne est par exemple un verre volcanique silicaté généralement légèrement translucide, mais noir. Le verre de REFIOM est également un verre d'oxydes, qui n'a rien de transparent.
Histoire
Bracelet en perles de verre, nécropole de Prosnes (Marne) culture de La Tène, V siècle avant notre ère.
Science
Histoire de la recherche
Les premières études scientifiques archéologiques sur le verre datent du XVIII siècle. Le premières recherches importantes furent effectuées par W.E.S. Turner et W. Geilmann au cours des années 1950. Les travaux de Edward Sayre et Robert Brill, du Musée du verre de Corning, publiées dans les années 1960, dominèrent la recherche durant 50 ans. À la fin du XX siècle, les archéologues s'intéressent de plus en plus au verre ancien, notamment à cause du développement de nouvelles méthodes d'analyse, du nombre grandissant de fouilles archéologiques de sites techniques et le développement de modèles interprétatifs se basant sur des analyses avec un objectif plus vastes.
Physico-chimie
Cette partie aborde le verre et ses caractéristiques d’un point de vue physico-chimique. Dans cette partie, nous limiterons notre étude à des verres d’oxydes. Cependant, il existe d’autres grands types de verres, en particulier, les verres métalliques (composés uniquement d’éléments métalliques) et les verres de spin (composés cristallisés caractérisés par une absence d’ordre magnétique à grande distance, d’où leur nom).
Structure
Le verre est un matériau amorphe, c’est-à-dire non cristallin. De ce fait, il présente un désordre structural important. Sa structure microscopique est telle qu’il n’existe aucun ordre à grande distance dans un verre. En cela, et en cela seulement, il est assez analogue à un liquide. Prenons l'exemple de l'eau pure, constituée de molécule d'H2O. Si on isole chaque molécule d'eau, autour de chaque atome d'oxygène, on trouvera toujours 2 atomes d'hydrogène: c'est un "ordre" (c'est reproductible d'une molécule à l'autre) à courte distance (à l'échelle de la molécule d'H2O). En revanche, si on prend deux molécules distinctes d'H2O en référence, à un instant t, et qu'on regarde leurs voisinages, c'est-à-dire où se trouvent, exactement les molécules d'H2O voisines de nos références, on obtiendra deux résultats complètement différents pour nos deux références. Il n'y a pas d'ordre à grande distance (à une distance supérieure à l'échelle de la molécule). On retrouve dans les verres cet ordre à courte distance (à l'échelle maximale de quelques distances interatomiques), mais pas au-delà.
Un verre peut même être vu comme un « réseau » tridimensionnel, semblable à celui d’un cristal, mais dans lequel seul l’ordre à courte distance est conservé. Comparons, par exemple, la structure de la silice (SiO2) cristalline (sous sa forme cristobalite) et celle de la silice vitreuse :
Représentation schématique bi-dimensionnelle de la silice cristalline (cristobalite).
Représentation schématique bi-dimensionnelle de la silice vitreuse.
Dans les deux cas, chaque atome de silicium est lié à quatre atomes d’oxygène, formant ainsi des tétraèdres SiO4 (c'est l'ordre à courte distance); chaque tétraèdre pouvant être considéré comme une « brique » de l’édifice final. Mais tandis que la cristobalite peut être définie comme un empilement régulier de ces briques SiO4 (elle a un ordre à grande distance), la silice vitreuse peut être considérée comme un empilement anarchique de ces mêmes briques SiO4 (elle n'a plus d'ordre à grande distance).
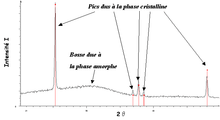
Diffractogramme de rayons X d’un mélange de deux composés : l’un vitreux et l’autre cristallin.
En raison de sa structure amorphe, les verres produisent, en diffraction des rayons X (DRX), un halo de diffusion, contrairement aux cristaux qui donnent des pics étroits et intenses.
Principaux composants
En raison de sa structure amorphe, le verre est soumis à très peu de contraintes stœchiométriques. De ce fait, un verre peut inclure en son sein une très grande variété d’éléments et présenter des compositions très complexes.
Dans un verre d’oxydes, ces différents éléments sont sous une forme cationique, afin de former des oxydes avec l’anion oxygène O.
Les cations intervenant dans la composition de verres peuvent être classés en trois catégories selon le rôle structural qu’ils jouent lors de la vitrification (formation du verre) : les formateurs de réseau, les non-formateurs de réseau (ou modificateurs de réseau) et les intermédiaires. Les critères structuraux de cette classification prennent en compte le nombre de coordination (nombre d’atomes d’oxygène auquel est lié le cation) et les forces de liaison.
Dans les verres non-oxydes (chalcogénures, verres métalliques…), on ne peut pas parler en termes de formateurs/modificateurs de réseau. On peut en particulier réaliser des verres avec un unique élément, comme le verre de soufre ou le verre de sélénium (qui sont les seuls éléments connus aujourd'hui pouvant former, seuls, un verre) : ces éléments ne sont donc classables ni comme formateurs, ni comme modificateurs. Une multitude de verres de chalcogénures peuvent être formés, dont germanium-sélénium, arsenic-sélénium, tellure-arsenic-sélénium. Pour ces verres, on ne parlera pas en termes de formateurs/modificateurs de réseau. Les verres métalliques sont généralement formés à partir d'au moins trois atomes ayant de grandes différences de rayon atomiques, de façon à rendre la cristallisation plus difficile, et l'obtention du verre possible avec des vitesses de trempe acceptables. Les verres métalliques n'ont pas de liaisons covalentes, et on ne parlera donc également pas en termes de formateurs/modificateurs de réseau.
Formateurs de réseau
Les formateurs de réseau sont des éléments qui peuvent à eux seuls former un verre. Les éléments formateurs les plus courants sont le silicium. Si (sous sa forme oxyde SiO2), le bore B (sous sa forme oxyde B2O3), le phosphore P (sous sa forme oxyde P2O5), le germanium Ge (sous sa forme oxyde GeO2) et l’arsenic As (sous sa forme oxyde As2O3).
Ce sont des éléments métalliques de valence assez élevée (généralement 3 ou 4, parfois 5), qui forment des liaisons iono-covalentes (mi-covalentes mi-ioniques) avec les atomes d’oxygène. Ils donnent des polyèdres de faible coordinence (3 ou 4), comme SiO4, BO4 ou BO3. Ces polyèdres sont liés par leurs sommets et forment le réseau vitreux.
Modificateurs de réseau
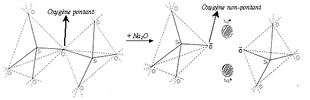
Rupture d’un pont Si-O-Si par adjonction d’une molécule de modificateur Na2O.
Les modificateurs de réseau (ou non-formateurs) ne peuvent pas former de verre à eux seuls. Ce sont essentiellement les alcalins, les alcalino-terreux et dans une moindre mesure certains éléments de transition et les terres rares.
Ils sont habituellement plus volumineux (rayon ionique plus important) que les formateurs de réseau, faiblement chargés et donnent des polyèdres de grande coordinence. Leurs liaisons avec les atomes d’oxygène sont plus ioniques que celles établies par les formateurs.
Ils peuvent avoir deux rôles structuraux bien distincts, soit modificateurs de réseau vrais, soit compensateurs de charge.
Les modificateurs de réseau vrais cassent les liaisons entre les polyèdres du réseau vitreux provoquant une dépolymérisation de ce dernier. Ils transforment alors les oxygènes pontants, qui lient deux éléments formateurs de réseau, en oxygènes non-pontants, liés à un seul formateur de réseau. Ceci se traduit à l’échelle macroscopique par une diminution du point de fusion et de la viscosité.
Les compensateurs de charge quant à eux compensent une charge négative sur un polyèdre formateur de réseau, par exemple BO4, lui permettant d’être stable dans cette configuration.
Intermédiaires
Les éléments intermédiaires ont différents comportements : certains de ces éléments sont soit formateurs, soit modificateurs selon la composition du verre tandis que d’autres n’auront ni l’une ni l’autre de ces fonctions mais un rôle intermédiaire.
Les principaux éléments intermédiaires dans les verres d’oxydes sont l’aluminium Al, le fer Fe, le titane Ti, le nickel Ni et le zinc Zn.
Centres colorés

Un verre de teinte bleue peut être obtenu avec un ajout de cobalt.
Des métaux et des oxydes métalliques peuvent être ajoutés lors du processus de fabrication du verre pour influer sur sa couleur.
L’ajout d’une faible quantité de manganèse permet d’éliminer la teinte verte produite par le fer. À des concentrations plus élevées, il permet l’obtention d’une couleur proche de celle de l’améthyste.
De même que le manganèse, le sélénium utilisé en faible quantité permet de décolorer le verre. Une quantité plus importante produit une teinte rouge. Le verre est teint en bleu par l’ajout d’une faible concentration de cobalt (0,025 à 0,1 %).
L’oxyde d’étain et les oxydes d’antimoine et d’arsenic permettent de produire un verre blanc opaque. Ce procédé a été utilisé pour la première fois à Venise pour obtenir une imitation de porcelaine.
L’ajout de 2 à 3 % d’oxyde de cuivre produit une couleur turquoise alors que l’ajout de cuivre métallique pur conduit à un verre rouge très sombre, opaque, parfois utilisé comme substitut au rubis doré.
Suivant la concentration utilisée, le nickel permet de produire des verres bleus, violets ou même noirs.
L’ajout de titane conduit à un verre jaune-brun.
L’or métallique ajouté à des concentrations très faibles (voisines de 0,001 %) permet d’obtenir un verre de couleur rubis, tandis que des concentrations plus faibles encore conduisent à un verre de rouge moins intense, souvent présenté comme « groseille ».
De l’uranium (0,1 à 2 %) peut être ajouté pour donner au verre une teinte jaune ou verte ou encore mauve, fluorescente appelé ouraline. Ce dernier n’est pas assez radioactif pour être dangereux. En revanche, s’il est broyé pour former une poudre, par exemple en le polissant avec du papier de verre, la poudre peut être cancérigène par inhalation.
Les composés à base d’argent (notamment le nitrate d’argent) permettent d’obtenir des teintes dans une gamme allant du rouge orangé au jaune. La couleur obtenue par l’ajout de ces différents additifs dépend de manière significative de la façon dont le verre a été chauffé et refroidi au cours du processus de fabrication.
Transition vitreuse
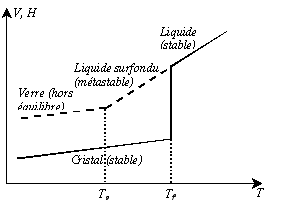
Variations thermiques du volume spécifique V et de l’enthalpie H lors du passage de l’état liquide à l’état solide (vitreux ou cristallin).
D’un point de vue thermodynamique, le verre est obtenu à partir d’une phase liquide surfondue solidifiée au point de transition vitreuse, Tg .
Pour une composition donnée, on s’intéresse à la variation d’une grandeur thermodynamique du premier ordre comme le volume occupé par cette phase (en maintenant la pression constante) ou une des fonctions thermodynamiques énergétiques molaires, comme l’enthalpie H, par exemple (on aurait aussi pu choisir l’énergie interne U).
Intéressons-nous au refroidissement d’un liquide. A priori, pour des températures inférieures à la température de fusion Tf (Tf dépend de la pression), l’état le plus stable thermodynamiquement correspond à l’état cristallisé (enthalpie la plus faible possible). À Tf, on observe alors une variation de H ou de volume: il s'agit d'une modification d'une grandeur thermodynamique du premier ordre, qui correspond à un changement d'état. Sous la Tf on observe aussi un changement de pente de H (cette pente est beaucoup plus faible pour un solide que pour un liquide).
Mais si, lors du refroidissement du liquide, la viscosité est trop importante ou le refroidissement très rapide, la cristallisation n’a pas le temps de se produire et un liquide surfondu est alors obtenu. Aucune discontinuité de H n’est alors observée à Tf et sa pente reste inchangée. En poursuivant le refroidissement, la viscosité du liquide augmente de façon exponentielle et le liquide surfondu devient quasiment solide. Lorsqu’elle atteint 10 poises, la rigidité empêche les mouvements microscopiques locaux et on observe un changement de pente de l’enthalpie: il n'y a pas de variation de grandeur thermodynamique du premier ordre, mais un changement de grandeur thermodynamique du second ordre comme le coefficient de dilatation, ou la capacité calorifique (qui s'observe par dilatométrie et calorimétrie différentielle à balayage respectivement). La température à laquelle se produit ce changement s’appelle température de transition vitreuse, Tg. La transition vitreuse est donc appelée "transition thermodynamique du second ordre" (par opposition à la fusion qui est une transition du premier ordre). La transition vitreuse résulte d'une perte de mobilités atomiques au fur et à mesure du refroidissement. Elle n'est pas intrinsèque et dépend donc de la vitesse de refroidissement: elle augmente si la vitesse de trempe augmente. Pour une température inférieure à Tg, le matériau est un solide avec le désordre structural d’un liquide : c’est un verre. Le désordre, et donc l’entropie, sont plus élevés dans un verre que dans un cristal. Sous la Tg, l'entropie (l'enthalpie ou le volume) varie de la même façon pour le verre et pour le cristal. Mais, en théorie, si le verre est refroidi suffisamment lentement, la Tg s'abaissant, par extrapolation de la variation d'entropie du liquide surfondu, on pourrait obtenir un verre d'entropie plus faible que le cristal équivalent: c'est ce qu'on appelle le paradoxe de Kauzmann. L'alternative à ce paradoxe reste débattue.
Le passage continu de l’état liquide à l’état vitreux se fait dans une plage de température délimitée par la température de fusion (Tf) et la température de transition vitreuse (Tg). La zone de transition vitreuse encadre Tg. En dessous de Tg, le verre devient "hors équilibre": il s'éloigne de son équilibre thermodynamique, puisque les mobilités atomiques ne sont plus suffisantes (la viscosité augmentant) pour que l'équilibre soit atteint (il s'éloigne donc d'autant plus de l'équilibre que la vitesse de refroidissement est élevée). Hors équilibre, on dit que le verre est l'isostructural d'un liquide de température plus élevée (ce qu'on appelle la température fictive). Le temps de relaxation nécessaire pour atteindre l’équilibre de configuration (l'équilibre thermodynamique) est alors supérieur au temps d’expérience. Ainsi, le verre est un matériau métastable, évoluant inévitablement vers l’état d'équilibre (jusqu'à ce que sa température fictive égale sa température effective).
Un liquide qui s'ignore ?
Le verre est souvent décrit comme un liquide extraordinairement visqueux et son caractère de solide est souvent discuté. Le verre est décrit comme un liquide qui s'ignore, car il aurait la propriété de couler à température ambiante. Rappelons tout d'abord que cette propriété n'est pas propre au verre : la glace, par exemple, pourtant solide cristallin, s'écoule à l'échelle des temps humains avec une viscosité à - 13 °C à peine supérieure à celle des verres à leur Tg. Rappelons ensuite que le caractère solide, en rhéologie, ne se définit que par rapport au temps d'observation. Le temps de relaxation mécanique d'un corps est défini, au sens de Maxwell, comme le ratio entre sa viscosité et son module d'élasticité en cisaillement. Il est de l'ordre de grandeur de l'inverse de la fréquence des mouvements atomiques associés à l'écoulement. Le nombre de Deborah est défini comme le ratio entre le temps de relaxation et le temps d'observation. Un corps est dit solide si ce nombre est très supérieur à 1, liquide sinon.
La plupart des verres silicatés ont des temps de relaxation à l'ambiante qui dépasse l'âge de l'univers, et donc des nombres de Deborah très supérieur à 1, même en considérant un temps d'observation de l'ordre de l'âge de l'humanité. Ce sont des solides au sens rhéologique. Ainsi d’après Daniel Bonn, du Laboratoire de physique statistique de l’ENS, si les vitraux des cathédrales ou les glaces de la Galerie des Glaces au château de Versailles sont plus épais à la base qu’à leur sommet, c’est du fait du procédé de fabrication utilisé, la partie la plus épaisse étant disposée vers le bas pour des raisons de stabilité. En revanche, certains verres, dont les verres de chalcogénures, ont des Tg relativement basses, proches de l'ambiante. C'est le cas du sélénium amorphe (sélénium noir) (Tg=42 °C), qui a un temps de relaxation à l'ambiante de l'ordre de 15 000 secondes (3,7 heures). L'écoulement du sélénium amorphe s'observe donc facilement à température ambiante bien qu'il soit sous sa Tg.
Résistance chimique et altération du verre
Le verre industriel a de bonnes compatibilités avec la plupart des composés chimiques, par contre l’acide fluorhydrique (HF) dégrade facilement le verre.
Les verres ne sont pas insensibles à l’action de l’eau ou de l’air. L'eau affecte la plupart des propriétés du verre, comme sa viscosité par exemple. Un des effets connus de l'eau sur le verre est la "propagation sous critique": par réaction d'hydrolyse, les fissures se propagent progressivement dans les verres sous contrainte, ceci pouvant conduire à leur rupture à plus ou moins long terme. Bien sûr, cela n’empêche pas l’existence de verres ayant plusieurs millions d’années et non altérés car la sensibilité des verres à l’altération dépend de leur composition chimique.
Résistance mécanique: fragilité
Le verre, au sens commun, apparaît comme un matériau fragile. Les verres silicatés, comme la plupart des verres d'oxydes ou de chalcogénures, sont effectivement fragiles à température ambiante dans le sens où ils peuvent être brisés sans générer la moindre déformation permanente (à l'inverse d'un matériau ductile, comme le plomb, qu'on peut déformer, plier, avant de le casser). Il est cependant possible de déformer un verre de façon permanente, sous haute pression: on parle de "densification". La silice vitreuse peut ainsi voir son volume réduit de près de 25%. Le caractère fragile des verres, donc l'absence de mécanisme de déformation plastique à température ambiante (en dehors de sous de hautes pressions), est dû à leurs liaisons atomiques fortes (covalentes ou ioniques en majorité). D'une manière générale, on s'attendrait à ce qu'un matériau ayant de fortes énergies de liaison soit très résistant mécaniquement, car il faudrait une grande énergie mécanique pour parvenir à rompre ses liaisons (le diamant est le matériau type qui soutiendrait cette idée). On sait aujourd'hui que la moindre rayure de surface sur ces matériaux va être l'initiateur d'une fissure et d'une rupture dramatique, par un phénomène de concentration de contrainte. Comme il est quasi-inévitable qu'un matériau dur comme le verre présente des défauts anguleux en surface, ce qui compte pour caractériser sa résistance mécanique n'est pas son énergie de liaisons atomiques, mais sa ténacité, c'est-à-dire la résistance à la propagation de ces défauts. La ténacité des verres d'oxyde est relativement faible (0,5-1,0 MPa.√m), soit quasiment cent fois moins que les métaux courants. La ténacité des verres silico-sodo-calciques peut cependant être considérablement augmentée par trempe thermique ou chimique. La plupart des écrans de smartphone et tablette tactile sont aujourd'hui des verres fins trempés chimiquement.
Calcul de propriétés
Valeurs représentatives
Les valeurs qui suivent ne sont destinées qu’à fournir un ordre de grandeur, car il existe plusieurs variétés de verres, des flints lourds (chargés en plomb ; masse volumique variant de 2 500 à 5 900 kg/m) au verre à vitre standard (2 500 kg/m) en passant par les crowns (de 2 200 à 3 800 kg/m), etc.
Propriétés physiques moyennes du verre sodique Propriété physique Valeur Unité Masse volumique 2 500 kg/m Module de Young 69 000 MPa Coefficient de Poisson 0,25 Limite d'élasticité 3 600 MPa Résilience de 1 500 à 2 500 Pa Coefficient de dilatation linéaire de 0,5 à 15×10 /°C Conductibilité thermique 1 W/m/°C
Calcul par combinaison des propriétés de différentes phases
Les propriétés de verre peuvent être calculées par l’analyse statistique des bases de données de verre, par exemple SciGlass et Interglad. Si la propriété de verre désirée n’est pas liée à la cristallisation (par exemple, la température de liquidus) ou à la séparation de phase, la régression linéaire peut être appliquée en utilisant des fonctions polynômes communes jusqu’au troisième degré. Au-dessous figure une équation d’exemple du deuxième degré. Les C-valeurs sont les concentrations composantes de verre comme Na2O ou CaO en pourcentage ou d’autres fractions, les b-valeurs sont des coefficients, et n est le chiffre total des composants de verre. La composante principale de verre, la silice (SiO2), est exclue dans l’équation ci-dessous en raison de l’au-dessus-paramétrisation, due à la contrainte que tous les composants résument à 100 %. Beaucoup de termes dans l’équation ci-dessous peuvent être négligés au moyen de l’analyse de corrélation et de signification.
Propriété du verre =
Autres verres
Par extrapolation le nom de verre est employé pour d’autres matériaux amorphes.
Par exemple, des mélanges à base de fluorures de zirconium, baryum, lanthane et aluminium produisent des verres fluorés plus transparents dans l’ultraviolet et le proche infrarouge que le verre de silice. Ils servent donc à fabriquer des instruments optiques pour ces rayonnements.
Beaucoup de verres de lunettes sont fabriqués avec des verres organiques qui sont des polymères à base de carbone comme le polycarbonate de bisphénol A ou le polycarbonate d’allyle.
Certains alliages métalliques peuvent être solidifiés avec une structure amorphe grâce à un refroidissement très rapide, on les appelle alors des verres métalliques. On peut par exemple projeter le métal en fusion sur un tambour de cuivre tournant à grande vitesse. Ces alliages sont utilisés par exemple pour les cœurs de transformateurs. En effet leur cycle d’hystérésis est très faible, ce qui réduit considérablement les pertes.
On peut obtenir des dépôts d’alliages métalliques (Al-Cu-Fe) amorphe par dépôt sous vide.
Certains aciers peuvent être solidifiés sous forme amorphe. Du fait de leur isotropie, ils ont des propriétés non-magnétiques intéressantes notamment pour la construction de sous-marins furtifs. Ils ont également une grande dureté et une très bonne tenue à la corrosion.
Verre naturel
Le verre naturel est tout type de verre formé naturellement. On distingue deux grandes familles : le verre biologique et le verre géologique.
Verre biologique
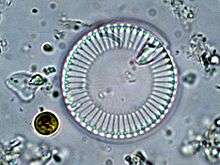
Cyclotella meneghiniana est une petite espèce commune de diatomée d’eau douce.
L’espèce produisant le plus de verre sur Terre n’est pas l’homme, mais la famille des diatomées. En effet, ces algues unicellulaires sont protégées par une coque de verre aux formes surprenantes et délicates. Constituant du plancton, ce verre a une masse considérable et bien supérieure à celle produite par les hommes. Depuis 2008, les scientifiques commencent à identifier le détail de la synthèse : elle part des silicates présents dans l’eau de mer, et ils commencent à savoir reproduire en laboratoire des réactions similaires. Cette fabrication a lieu dans des conditions physiques de la chimie douce, c’est-à-dire qu’elle ne nécessite ni température ni pression élevées.
L’intérêt majeur du verre pour la diatomée est de ne pas faire obstacle à la photosynthèse en laissant passer la lumière. Il est synthétisé très rapidement au moment de la méiose.
Verre géologique
De nombreuses roches silicatées, si elles sont refroidies suffisamment rapidement, ont tendance à vitrifier. On observe en particulier ce phénomène, sur Terre, auprès des volcans, où on peut par exemple observer la formation d'obsidienne, de pierres ponces (de composition généralement proche de l'obsidienne), de tachylyte, de palagonite…
Les fulgurites sont un autre exemple de verre naturel produit par un impact de foudre (généralement sur le sable). L'impactite se forme, elle, par l'impact d'un météorite. Sa forme la plus connue est le verre lybique. La Lune possède également, à sa surface, de la roche vitrifiée par des impacts de météorites. On parle alors de verre lunaire.
Les comètes seraient également constituées, de "verre d'eau" ou glace amorphe.
Verres bioactifs
Les verres bioactifs, ou bioverres, sont des matériaux utilisés en chirurgie réparatrice comme substituts osseux. Voir l'article verres bioactifs
Production
En dehors de films minces, déposés suivant diverses méthodes, le processus de synthèse de verre est très souvent le suivant : fusion, trempe et recuit (la méthode de "fusion-trempe" ou "melt quenching method", en anglais). Concernant les verres silico-sodocalciques, les éléments nécessaires à la synthèse du verre, généralement des oxydes (silice) et des carbonates (carbonates de calcium, de sodium) sont mélangés puis amenés à fusion. Pour le verre à vitre standard, on utilise du sable blanc, de la soude, de la chaux et du verre cassé (le calcin) qu'on porte à 1 550 °C. Le verre est ensuite souvent affiné, surtout pour des volumes importants: on le débarrasse de ses bulles en le maintenant à haute température. La viscosité assez faible favorise alors la remontée des bulles à la surface. On peut également passer par un processus d'homogénéisation, en mélangeant par exemple le liquide, si les mouvements de convection au sein du liquide ne suffisent pas. Le verre est ensuite trempé, c'est-à-dire refroidi brutalement pour permettre la vitrification. Pour la plupart des verres silicatés, une trempe à l'air ambiant suffit. Les verres métalliques nécessitent des trempes plus violentes, puisque le refroidissement doit parfois atteindre plusieurs milliers de kelvins par seconde. La trempe induit un refroidissement plus rapide de la surface du verre (en contact avec l'air) que du cœur, et donc des contraintes résiduelles. Ces contraintes détériorent considérablement la tenue mécanique du verre. Pour les relaxer, le verre est recuit à une température proche de la Tg, pour des durées qui varient selon la nature et le volume de verre.
Mise en forme
Le verre peut être mis en forme selon différentes méthodes qui peuvent être classées en continues et en discontinues :
Classe Procédé Définition Exemples Discontinu Soufflage Verre creux Coulage dans un moule Le verre fondu est versé dans un moule ayant la forme de l'objet à fabriquer Verre creux Pressage Le verre fondu est comprimé dans un moule ayant la forme de l'objet à fabriquer Tube cathodique, verre creux Coulée par centrifugation Verre creux Continu Laminage Le verre fondu est passé entre deux cylindres lamineurs Verre plat (procédé peu utilisé) Étirage Verre plat (procédé peu utilisé), tube luminescent, fibre de verre Flottage Le verre fondu est versé sur un bain d'étain liquide et s'y étale en formant un ruban continu Verre plat Coulage sur table Le verre fondu est versé sur une table et laminé Verre plat (procédé peu utilisé) Extrusion
Utilisation

Bouteille pour eau minérale.

Diverses présentations utilisées notamment comme renfort de plastiques ou de composites.
Escalier en verre de l'Apple Store d'Amsterdam.
Le verre est utilisé essentiellement en optique pour ses propriétés réfringentes (lentilles, verres de lunettes). Les verres d'oxydes sont connus pour leur application en optiques dans le visible et le proche infrarouge (lentilles, prismes, fibres, miroir) et en télécommunication (fibre optique). La transparence des verres silicatés en font un élément majeur dans le développement de l'énergie solaire. Les verres de chalcogénures se développent aujourd'hui pour des applications d'optique infrarouge, dont la vision nocturne, la spectroscopie infrarouge par onde évanescente, des applications d'holographie, d'optoélectronique… Les verres de chalcogénures sont également massivement utilisés dans le DVD où ils sont supports de l'information.
Il est également utilisé en chimie et dans l’industrie agroalimentaire : il réagit très peu avec la plupart des composés utilisés dans ces domaines, c’est donc un matériau idéal pour les contenants (bouteilles, pots de yaourt, béchers, erlenmeyers, colonnes de distillation, éprouvettes, tubes à essai). Un des seuls liquides ayant le pouvoir de dissoudre le verre est l’acide fluorhydrique (HF).
Le verre est le matériau dans lequel sont confinés les déchets radioactifs de haute activité (HAVL) par le procédé de vitrification. Étant désordonné, le verre supporte en effet bien les radiations sur le long terme, à l'inverse des métaux dont la structure a justement tendance à s'amorphiser et donc à perdre ses propriétés mécaniques sous irradiation. De plus, le verre vieillit très bien à l'échelle géologique, même en présence d'eau.
Le verre est aussi un matériau de construction très important dans l’architecture moderne et dans l’industrie automobile. Il est notamment présent sous forme de laine de verre, isolant léger, imputrescible et ininflammable et la brique de verre est utilisée pour réaliser des parois translucides. L'émergence des verres métalliques a permis d'introduire des verres comme matériaux de structure, du fait de leurs extraordinaires propriétés mécaniques, en particulier sous forme de fibres ou de rubans de renfort pour des bétons hautes performances. Les verres métalliques se sont également introduits dans les articles de sports (raquettes, skis, battes). Les fibres de verres vont également jouer un rôle important dans les ouvrages architecturaux futurs, en étant tantôt des éléments de renfort mécanique et tantôt des guides optiques véhiculant l'information des différents capteurs permettant la surveillance continue des ouvrages.
Le verre est également présent dans les éléments de haute technologie du quotidien: disques durs, écrans tactiles, verres autonettoyants, et les industriels du verre envisagent de multiples applications futures.
Les utilisations artistiques du verre sont innombrables depuis les origines. Elles ont accompagné de nombreuses innovations techniques (pâte de verre, fusing, thermo-formage, etc).
Dans de nombreuses applications, le verre est actuellement remplacé par des matières plastiques, plus légères et souvent plus résistantes au choc.
On peut le rencontrer sous forme de microbilles, de fibres (coupées ou non), de mats (fibres disposées « en vrac ») ou de tissus (mode de tissage « taffetas », par exemple). Incorporées dans la matrice polymère ou déposées en surface, ces présentations sont utilisées notamment comme renfort (fibreux ou non) de résines thermoplastiques (polyamides) ou thermodurcissables (polyesters, époxydes) dans les plastiques, ainsi que dans les matériaux composites.
Types de verres industriels
Verre plat : Verre « float » ou verre flotté Verre coulé
Verre « float » ou verre flotté
Verre coulé
Verre creux : Verre moulé : utilisé surtout pour fabriquer des bouteilles. Verre étiré : produit semi-fini permettant de réaliser des ampoules, des flacons ou de la verrerie de laboratoire.
Verre moulé : utilisé surtout pour fabriquer des bouteilles.
Verre étiré : produit semi-fini permettant de réaliser des ampoules, des flacons ou de la verrerie de laboratoire.
Le verre peut subir des modifications pour le renforcer et le sécuriser :
Verre trempé : Trempe thermique : Des traitements thermiques permettent d’améliorer la résistance des pièces : les vitres latérales et arrières des automobiles comme certaines pièces d’ameublement sont trempées par un refroidissement rapide et contrôlé, le plus souvent par de l'air. Trempe chimique : Ce type de trempe a lieu en remplaçant par diffusion une partie des ions alcalins par d'autres ions alcalins de plus gros rayon ionique. Par exemple le sodium ou le lithium du verre par des ions potassium.
Trempe thermique : Des traitements thermiques permettent d’améliorer la résistance des pièces : les vitres latérales et arrières des automobiles comme certaines pièces d’ameublement sont trempées par un refroidissement rapide et contrôlé, le plus souvent par de l'air.
Trempe chimique : Ce type de trempe a lieu en remplaçant par diffusion une partie des ions alcalins par d'autres ions alcalins de plus gros rayon ionique. Par exemple le sodium ou le lithium du verre par des ions potassium.
Verre feuilleté : Composé de couches verre-plastique-verre ou plus. Les pare-brises des automobiles et les vitres blindées sont en verre feuilleté. Ainsi, lors d’un choc, le pare-brise se casse, mais reste en place. Les passagers risquent moins d’être blessés par des bris. Le verre blindé ayant 8 couches de plastique peut résister à 70 coups de hache avant d'être traversé.
Le verre peut aussi subir des traitements de surface, le plus souvent des dépôts :
Verre antireflet : Verres de lunettes de vue
Verre hydrophobe : Pare-brises et miroirs…
Techniques artisanales du verre
La verrerie constitue une activité artisanale.
Travail du verre à la flamme « souffleur de verre au chalumeau » : les verriers travaillent à partir de tubes et de baguettes de verre étiré qu’ils ramollissent à l’aide de la flamme d’un chalumeau pour le transformer par le souffle ou par différents outils. En France, le travail du verre soufflé, à la flamme, pour la réalisation d’objets décoratifs ou utilitaires, ou de pièces uniques est pratiqué par plusieurs artisans.
Verre soufflé: les souffleurs de verre font chauffer une boule de verre au bout d’une canne dans laquelle ils soufflent pour faire gonfler le verre et réaliser une boule vide. Ensuite, ils étirent, aplatissent, percent cette boule pour lui donner sa forme finale. Une fois durci, certains le dépolissent pour réaliser des motifs.
Verre bombé : déformé à la température de ramollissement (≈ 600 °C) sur la courbure d'un moule, ce procédé de bombage peut être combiné à la trempe, au feuilletage, de manière artisanale (bombeur de verre fabriquant des lampadaires, vitrines d'argentier, globes d'horloges) ou industrielle (pare-brise et lunettes automobiles, miroirs optiques).
Depuis l'Antiquité, les artistes-peintres ont adopté la feuille de verre comme support pour peindre; entre autres la peinture sur verre inversé (ou peinture sous verre ou peinture sur verre) est une technique artistique difficile qui s'exécute directement sur une feuille de verre. Le verre supporte la peinture comme le ferait une toile. Soudée au verre, c'est à travers ce support que l'on contemple l'œuvre. Ainsi le verre sert à la fois de support et de vernis protecteur. Précisons que c'est une technique de peinture à froid de sorte que le procédé n'exige pas de cuisson au four. Le pigment est lié au verre par un véhicule huileux le plus souvent à base de vernis.
Terminologie
Cristal : verre à haute teneur en plomb qui lui donne un éclat plus intense et se travaille de façon similaire au verre. Pour mériter l’appellation de cristal, la concentration en oxyde de plomb doit être comprise entre 24 et 56 %.
Pâte de verre : le moule de la pièce à réaliser se fabrique dans un matériau réfractaire (à base de kaolin par exemple) selon diverses techniques dont la cire perdue. Après cuisson, selon des paliers de chauffe destinés à éviter les fissures, le moule est refroidi et garni de poudres ou de granulés de verres colorés diversement selon le décor recherché. Une nouvelle cuisson a lieu et, après refroidissement, le moule est détruit délicatement par un moyen chimique ou mécanique pour dégager la pièce dont la forme et les couleurs auront été parfaitement contrôlées. Cette technique attribuée aux Égyptiens, a été réinventée presque simultanément par Henry Cros, François Décorchemont et Georges Despret dans la deuxième partie du XIX siècle. Almaric Walter, Gabriel Argy-Rousseau s’y sont illustrés.
Thermoformage : cette technique consiste à poser à froid une (ou plusieurs) feuilles de verre, éventuellement colorées, sur un réfractaire dont elle épousera le relief à la cuisson.
Fritte : composition de verre, pouvant être colorée (à l’aide d’oxydes métalliques), portée à fusion et trempée dans un bain d’eau froide afin de la réduire en granulés servant à l’élaboration d’émaux ou de « ballottes » (barres) colorées, matériaux de base des verriers.
Cueiller : action de prélever une masse de verre dans le four à l’aide d’une canne ou d’un pontil.
Pontil : tube métallique plein, le pontil permet une mise en forme au « marbre » ou à l’aide de divers outils. Il sert aussi à la séparation de l’objet de la canne afin de percer et travailler le col, à rapporter des éléments de décor, des anses, un pied.
Recyclage
Le verre, s’il est bien trié (Tri sélectif) peut se recycler indéfiniment sans perdre ses qualités. Dans certains pays tels que l'Allemagne, la Belgique, la Suisse ou les pays nordiques, le tri peut différencier le verre blanc, vert et brun pour un recyclage plus performant, et les bouteilles consignées puis réutilisées sont plus fréquemment choisies par les producteurs et consommateurs.
Refonte

Conteneur destiné à accueillir du verre brisé à recycler (fonte).
Les bouteilles de verre usagées peuvent être fondues. La matière ainsi récupérée permet de fabriquer de nouvelles bouteilles.
Le verre peut également être produit à partir de calcin (verre broyé) de récupération. La fabrication du verre à partir de calcin de récupération économise des matières premières et de l’énergie.
Avant d’être refondu, le verre subit différents traitements : broyage, lavage, élimination des colles, étiquettes, capsules, séparation du verre et des métaux et élimination des rebuts (porcelaine, cailloux…).
En France, le gros du verre est récupéré sous forme de verre brisé. Le verre consigné est récupéré dans l'ensemble des bars et cafés, ainsi que pour les bouteilles de bière en vente publique en Alsace. L'agence de l'environnement et de la maîtrise de l'énergie (ADEME) pense que le bénéfice de la consigne de contenants en verre n'est pas évident, compte tenu des circuits d'approvisionnement assez longs en France.
Consigne
Avec ce système les bouteilles sont récupérées entières, moyennant une contrepartie financière, lavées puis réutilisées.
En Europe, la consigne du verre re-remplissable est autorisée à la discrétion des États membres, à condition de ne pas générer de distorsions de concurrence et dans le cadre d'une politique de protection de l’environnement.
L’Allemagne et la Belgique ont privilégié la consigne. Le Canada utilise un système similaire à l’Allemagne et a uniformisé le format des bouteilles de bière pour faciliter une réutilisation plus rentable et facile par diverses compagnies.
Autres utilisations
En Guyane, depuis fin 2006, les déchets de verre (70 tonnes collectées de fin 2006 avec un premier chantier-test mi 2007 au centre de Cayenne) sont utilisés en fond de couche routière. Il faut 4 600 t de verre pour 30 km de route. Ce type de réutilisation peut cependant poser des problèmes de dangerosité (lors des chantiers et pour la faune fouisseuse).
Transparence
Certains verres sont transparents dans le visible, c'est notamment le cas de la plupart des verres silicatés, et c'est l'une des propriétés les plus exploitées des verres. D'autres verres sont transparents dans d'autres gammes de longueurs d'onde, comme les verres de chalcogénures. Le verre à vitre courant est transparent de l'UV jusqu'au moyen infrarouge, il ne transmet pas les UV-B et les UV-C. Ainsi, on peut bronzer derrière une vitre, puisque les UV-A sont transmis, mais très difficilement attraper des coups de soleil. Les verres qui sont transparents ne le sont toujours que dans une certaine gamme de longueurs d'onde, limitée aux basses longueurs d'onde par l'énergie de bande interdite et aux hautes longueurs d'onde par la coupure multi-phonon.
Les verres silicatés, du fait du silicium, possèdent une large bande interdite séparant la bande de valence de la bande de conduction (9 eV pour la silice vitreuse, entre 1 et 3 eV pour les verres de chalcogénures). Pour qu'un photon soit absorbé par le verre il doit avoir une énergie suffisante pour exciter les électrons de valence vers la bande de conduction. Si le photon a une énergie trop faible (une longueur d'onde trop grande) pour permettre à un électron de franchir la bande interdite, il est transmis et le verre est transparent à cette énergie de photon.
Du fait du désordre qui caractérise un verre, les bandes de valence et de conduction s'étendent dans la bande interdite (ils forment ce qu'on appelle des queues de bandes) et réduisent l'énergie séparant bande de valence et bande de conduction. La limite optique d'absorption (limite basse, en longueur d'onde, où le verre commence à transmettre) n'est donc pas abrupte (il n'y a pas un seuil précis d'énergie de photon pour laquelle la transparence commence) mais progressive, une fraction infime des photons pouvant être absorbés même à des énergies bien plus faibles que l'énergie de bande interdite. Cette zone de faible absorption correspond à la "queue d'Urbach".
À la vibration du réseau atomique on associe également une quasi-particule appelée phonon. Les phonons interagissent de diverses façons avec les photons (voir la diffusion Raman et la diffusion Brillouin). Des phonons peuvent interagir entre eux et générer un moment électrique qui affectera le rayonnement électromagnétique: c'est ce qu'on appelle l'absorption multi-phonons. Aux longueurs d'ondes élevées (énergies faibles) les verres ne transmettent donc plus du fait des interactions photons-phonons. Dans les verres silicatés, la vibration d'élongation de la liaison Si-O correspond à une longueur d'onde de 8,9 μm, et le verre absorbe donc énormément à cette longueur d'onde. Tellement que la première harmonique (fréquence double, donc longueur d'onde deux fois plus faible: 4,5 μm) produit déjà une très forte absorption.
La fréquence de vibration d'un réseau atomique, et donc l'énergie de phonon, est inversement proportionnelle à la masse des atomes et les éléments chalcogènes étant relativement lourds, ils repoussent la limite de transparence à des plus grandes longueurs d'onde (des plus faibles énergies) que les verres silicatés, et les verres de chalcogénures sont donc transparents plus loin dans l'infrarouge que les verres silicatés.
Les verres métalliques possèdent des électrons libres, ils sont conducteurs et n'ont donc pas de bande interdite. En conséquence, ils ne sont pas transparents. Chaque type d'impureté dans le verre va induire une ou plusieurs bandes d'absorption qui perturbe la transparence du verre. Pour le verre à vitre, le fer (ses oxydes) est l'impureté qui génère la teinte vert-bleutée que l'on peut déceler en regardant une vitre sur la tranche. Des verres contenant énormément d'impuretés, comme le verre de REFIOM, ne sont pas transparents mais noirs.
Symbolique
Le verre est un des premiers matériaux mis au point, rêvé par l’homme. Il est le symbole de la fragilité, la finesse et la transparence : par exemple, la pantoufle de verre de Cendrillon dans le conte de Charles Perrault et le dessin animé de Walt Disney. Il est souvent considéré que dans le conte original, la pantoufle était de vair, mais Perrault a écrit sa version de l’histoire avec une pantoufle de verre, le dessin animé reprend également cette idée.
Dans l'univers des Elder Scrolls, le verre est un minerai volcanique précieux utilisé pour forger en particulier des armes et des armures. Elles sont efficaces, mais paradoxalement fragiles. Cependant, dans le dernier opus, Skyrim, aucune précision n'est donnée sur sa solidité, étant donné que la dégradation de l'équipement n'est plus pris en compte dans le jeu.
Impacts de projectiles
Le verre selon son épaisseur, sa composition et son mode de production est plus ou moins résistants aux chocs, chutes et impacts.
Il a été montré que pour un verre donné, le nombre de fissures en étoile compté autour d'un point d'impact (de balle par exemple) traduit la vitesse relative du projectile contre le verre au moment de l'impact. En cas d'accident ou d'utilisation d'arme à feu ayant percuté du verre, il devient donc possible d'obtenir des informations sur la vitesse du projectile (et donc sur la distance du tireur si on connait le type d'arme et de munition utilisées) ; selon des tests ayant porté sur des projectiles lancés à une vitesse de plus en plus élevée jusqu'à 432 km/h, plus la quantité d'énergie cinétique est importante, plus le nombre de fissures est important, avec une équation simple reliant ces deux paramètres. Inversement, on peut maintenant déduire aussi la vitesse d'un véhicule au moment d'un accident, par l'observation des fissures d'un phare ou pare-brise perforé lors de l'accident.

 词典释义:
词典释义:





 酒杯
酒杯
 , 嵌丝
, 嵌丝








 , 磨
, 磨







 , 防弹
, 防弹






 , 安全
, 安全


 , 淬火
, 淬火


 纤维布 [供过滤或绝缘
纤维布 [供过滤或绝缘
 ]
] 纸
纸
 瓶
瓶
 工业
工业
 一样容易碎
一样容易碎
 片(或板、块等); pl.(光学)
片(或板、块等); pl.(光学)




 灯罩
灯罩
 表蒙
表蒙
 片
片
 镜框里
镜框里
 酒杯;
酒杯;
 杯;pl.
杯;pl. 
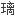 器皿
器皿
 酒杯
酒杯
 器皿
器皿
 物质
物质


 碎片
碎片




 的透明度
的透明度
 杯的裂痕
杯的裂痕


 的回收利
的回收利
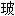
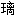 ;镜子
;镜子
 [制品];
[制品]; 
 ; 镜; 透镜
; 镜; 透镜


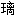 ; 夹丝
; 夹丝































































 剂量计
剂量计








































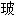
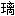




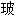


 封装
封装
 混凝土
混凝土
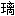 球
球 壳显像管
壳显像管
 刀
刀
 刀
刀
 漏斗
漏斗
 棉
棉
 纤维
纤维
 纤维
纤维
 棉
棉
 砖墙
砖墙
 冷凝器
冷凝器
 粗
粗

 沫
沫
 沫
沫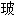
 蛇
蛇
 增强聚酯层压品
增强聚酯层压品
 纤维织品,
纤维织品, 
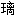 纤维
纤维
 布油毡
布油毡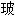
 管
管









