
Cristaux
Cristaux de sel obtenus par cristallisation lente dans une saumure à température ambiante.
Un cristal est un solide dont les constituants (atomes, molécules ou d'ions) sont assemblés de manière régulière, par opposition au solide amorphe. Par « régulier » on veut généralement dire qu'un même motif est répété à l'identique un grand nombre de fois selon un réseau régulier, la plus petite partie du réseau permettant de recomposer l'empilement étant appelée une maille .
Les cristaux les plus communs sont la neige, le sucre, les sels, les silicates, les oxydes, les sulfures, les métaux et les pierres précieuses (gemmes).
On appelle phénocristal un cristal de taille exceptionnelle, mais la plupart des cristaux qu'on observe sont composés de plusieurs cristaux accolés (ou cristallites). Dans le premier cas on parle de « monocristal » et dans le second de « polycristal». Un monocristal dont l'une des dimensions est inférieure à 100 nm est une nanoparticule qu'on appelle aussi nanocristal. Si cette dimension est réduite au minimum, c'est-à-dire à une seule couche d'atomes, on observe un cristal monoplan, tel le graphène.
Un cristal idéal ne comporte pas de défauts cristallins, mais les cristaux réels sont loin de cette perfection. Au-delà d'une certaine concentration des défauts, le concept de structure cristalline cesse d'être utile et l'on considère que c'est un matériau amorphe tel que le verre. L'état amorphe s'apparente fortement à l'état liquide mais il existe aussi des cristaux liquides.
Selon l'Union internationale de cristallographie, tout solide dont le diffractogramme est essentiellement discret est un cristal. Sur la base d'une propriété structurelle essentielle, cette définition englobe les cristaux classiques mais aussi les quasi-cristaux. Les propriétés des cristaux s'expliquent par leur composition atomique et l'arrangement spatial des atomes.
Historique
L'observation des cristaux est loin d'être récente. Déjà les Égyptiens connaissaient la turquoise et les gemmes (diamant, saphir, émeraude, rubis) étaient très appréciés au temps de l'antiquité. Strabon invente le mot Krystallos pour désigner le quartz. Il est évident que les cristaux ont toujours fasciné tant par leur aspect translucide et coloré que par leur forme facettée. Ces deux aspects sont intimement liés aux propriétés physiques propres aux cristaux et au fait qu'ils soient ordonnés. Cependant cet ordre est resté fort longtemps incompris. L'histoire de la cristallographie s'étale principalement sur deux siècles (XIXetXX siècles).
À partir de la fin du XVIII siècle, l'approche que l'on va avoir du monde des cristaux va être d'ordre purement géométrique, inspirée en cela par l'extrême rigidité du monde minéral. Domaine réservé tout d'abord aux naturalistes, la cristallographie va prendre son envol en France essentiellement au cours des XIXetXX siècles et sera marquée principalement par trois figures : Jean-Baptiste Romé de l'Isle, René Just Haüy et Auguste Bravais.
La science classique des cristaux
Romé de l'Isle, en reprenant les travaux de Sténon, remarque en 1772 que, bien que les faces des cristaux soient en général de tailles différentes du fait même de leur croissance, deux faces adjacentes forment toujours entre elles des angles égaux. Cette loi tout à fait générale ouvre la voie à une description unique de l'ensemble des cristaux en termes purement géométriques. Cependant il n'arrivera pas à déterminer l'ensemble des formes à partir de ce principe unique.
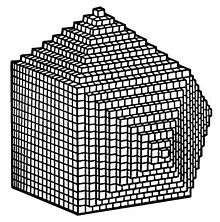
Construction de Haüy
C'est l'abbé René Just Haüy qui va réaliser le bond en avant et ceci par une découverte fortuite. En faisant tomber un cristal de calcite, il découvre qu'en se brisant, les fragments de tailles différentes présentent toujours le même caractère de facette que le cristal d'origine. Haüy en déduit que le cristal d'origine peut être décrit par un empilement de « molécules » semblables qu'il nomme « molécule intégrante ». Celles-ci, de forme parallélépipédique, s'emboîtent parfaitement pour constituer un solide homogène. D'après ce principe, la forme d'un cristal va dépendre du nombre d'éléments le composant, de sorte que les faces du cristal soient formées de minuscules gradins. En effectuant ainsi ce qu'il appelle le « décroissement égal sur tous les sommets », et qui consiste simplement à enlever des parallélépipèdes en nombre décroissant à partir des sommets ou d'une arête de la forme complète, il explique un grand nombre de formes naturelles (par exemple à partir d'un cube, on peut par décroissement à partir des sommets obtenir une morphologie octaédrique, comme celle de la fluorine). Il retrouve ainsi la loi de Romé de L'Isle sur la constance des angles puisque pour un empilement les angles sont conservés, et explique du même coup la notion de clivage.
Son travail ne s'arrête pas là puisqu'il trouve de façon mathématique que beaucoup de formes idéalisées peuvent être décrites par trois types de parallélépipédiques, dits primitifs. Du même coup, il montre l'impossibilité de construire un cristal avec des prismes pentagonaux, octogonaux. Gabriel Delafosse, élève d'Haüy, remplacera le terme de molécule intégrante par celui de « maille élémentaire », terme qui passera à la postérité. Cependant, les déductions d'Haüy ne sont pas complètes pour décrire l'ensemble des structures cristallographiques. Ceci nous amène à la définition du cristal, plus précisément du réseau cristallin, comme étant la répétition d'une maille élémentaire dans les trois directions de l'espace, avec la notion de pavage : un cristal est un objet périodique.
Les travaux d'Haüy vont être repris par Weiss lequel va recenser les faces d'un cristal par rapport à des éléments de symétrie. Ce principe très important en physique va guider toute la cristallographie. Ainsi, pour passer d'une face à l'autre, il est possible d'appliquer une opération de symétrie qui peut être une rotation, une inversion par rapport à un centre.
En 1848, Auguste Bravais rend une étude purement mathématique sur la classification des cristaux. Il décrit l'ensemble des structures possédant des symétries d'orientation compatibles avec la triple périodicité des cristaux dans les trois directions de l'espace (symétrie de translation). Il trouve ainsi 32 classes de symétrie réparties en 14 types de réseaux, les réseaux de Bravais que l'on peut regrouper en 7 systèmes définissant la forme de la maille élémentaire. Cette analyse affirme simplement que l'on ne peut disposer les points d'un réseau de façon arbitraire. Prenons le cas plus simple d'un réseau du plan (les résultats se généralisent à 3D).
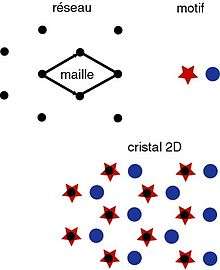
Réseau + motif = cristal
L'ère purement géométrique venait de finir, elle avait permis la classification exhaustive de l'ensemble des structures, reste à savoir ce qu'était véritablement une structure réelle. En cette fin de XIX siècle, la physique est en ébullition tant le concept d'atome bouleverse les règles établies. La théorie atomiste naissante est en partie bâtie à partir des conclusions fournies par la cristallographie. Gabriel Delafosse, en introduisant le concept de maille, avait déjà pressenti que l'on pouvait dissocier organisation et composant élémentaire : le cristal peut être décrit par une maille élémentaire décorée par un motif atomique.
La découverte de la nature réticulaire des cristaux, c'est-à-dire le fait que l'on puisse décrire les structures comme un ensemble de familles de plans (un empilement de couches d'atomes), chaque plan d'une même famille étant séparé d'une distance constante, la distance interréticulaire, a des conséquences importantes. Elle est due à Max von Laue qui découvre que les rayons X sont diffractés par la matière cristalline. Ce phénomène a lieu lorsque la taille de la fente par laquelle on fait traverser un rayonnement est de l'ordre de la longueur d'onde. Pour un cristal, la distance entre deux plans est de l'ordre de la distance entre atomes, c'est-à-dire 1/10 de milliardième de mètre. Dans ce cas pour obtenir le phénomène de diffraction, il faut un rayonnement dont la longueur d'onde est très courte. Cette condition est réalisée par les rayons X et c'est grâce à eux que l'on peut sonder la matière ! En particulier lorsqu'on éclaire un cristal dans une orientation particulière, le rayonnement n'est diffracté que dans des directions spécifiques : on obtient des clichés dits de diffraction, un réseau de taches qui a les mêmes symétries que le cristal.
Maille du chlorure de sodium : un atome de chlore (vert) et un atome de sodium (bleu) forment le motif élémentaire qui se retrouve aux sommets et aux centres des faces d'un cube.
Le travail de caractérisation des structures cristallines fut alors engagé par William Lawrence Bragg aidé par son père Sir William Henry Bragg (découverte pour laquelle ils reçurent le prix Nobel en 1915) et ne cessa de se développer avec un grand succès.
Il a ainsi été possible d'identifier un grand nombre de structures. Par exemple, les métaux cristallisent selon trois types de réseaux : cubique centré (fer, chrome), cubique à faces centrées (aluminium, cuivre), et hexagonal compact (zinc, titane). D'autres structures cristallisent aussi. C'est par exemple les protéines, les virus. L'exemple le plus célèbre est celui de la molécule d'ADN, constituant élémentaire de nos cellules. En 1953, Crick et Watson découvrent la structure en double hélice de cette molécule grâce à l'analyse des clichés de diffraction réalisés dans l'ombre par R. Franklin de la molécule cristallisée.
Le sel de mer est lui aussi un cristal : celui de chlorure de sodium (NaCl) qui cristallise selon un réseau cubique faces centrées. Dans ce cas on comprend mieux la notion de maille et de motif atomique décorant la maille.
La science contemporaine des cristaux
Au début des années 1980, travaillant sur un alliage d'aluminium et de manganèse rapidement solidifié Dan Shechtman obtint un spécimen cristallin qui présentait un cliché de diffraction très particulier. Le cliché était très net, ce qui indiquait une structure cristalline, mais il présentait une symétrie pentagonale qui selon la théorie bien établie était impossible. Différentes explications furent avancées mais bientôt il fallut se rendre à l'évidence : une nouvelle variété de cristaux avait été découverte. Trois autres chercheurs, I. Blech, J. W. Cahn et Denis Gratias ont signé avec Schechtman l'article fondateur, paru en 1984. Cette publication signale le début d'une véritable révolution scientifique : d'abord une controverse, amenant bientôt un renversement d'opinion, que suit la découverte rétrospective des cas occultés auparavant. Les cristaux classiques et bien connus sont depuis considérés comme un cas particulier : ce sont des cristaux périodiques. Dans une autre catégorie, on classe les cristaux apériodiques, où sont inclus les cristaux incommensurables reconnus avant la découverte de ceux qu'on appelait quasi-cristaux. Au début des années 1990, l'Union internationale de cristallographie a adopté une nouvelle définition de son objet principal, le cristal. Ainsi, on admet maintenant que la périodicité est une composante suffisante mais non nécessaire à l'ordre cristallin.
Cristallisation
Un cristal se forme si la température d'une coulée descend assez lentement sous le point de fusion et que le mouvement thermique des différents atomes atteint une valeur si faible que les connexions réciproques ne peuvent plus être fracturées par des oscillations - on vient en formation d'un treillis uniforme qui est marqué par un ordre à distance. Ce treillis uniforme a une plus faible enthalpie libre que le verre amorphe, qui se dispose seulement selon un ordre local (la disposition locale des atomes ne se répète pas régulièrement dans un verre) . On qualifie ce processus de cristallisation. Dans les cas où la température d'une coulée descend rapidement, différents phénomènes sont observés et les solides ainsi obtenus peuvent avoir des propriétés bien particulières.

 词典释义:
词典释义:


