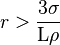La solidification est l'opération (plus ou moins réversible) au cours de laquelle un liquide passe à l'état solide.
Cela peut se faire par refroidissement (cas le plus courant), par augmentation de la pression, par cristallisation, par catalyse ou bien par une combinaison de ces phénomènes. La congélation peut aussi permettre la solidification de certains fluides (l'eau par exemple).
La solidification de l'eau pure se fait à une température de 0°C.
Enjeux industriels
Il y a de très nombreux enjeux et applications industrielles à la bonne compréhension et maîtrise des phénomènes de solidification : coulée continue d'acier, croissance du Si pour l'électronique, moulage d'implants dentaires...
La solidification se fait en général par précipitation ou cristallisation à partir de la formation de germes de phase solide au sein du liquide (germination, nucleation en Anglais) puis croissance de ces germes ; avec donc une redistribution des éléments chimiques (quand la matière n'est pas mono-élémentaire).
À pression constante, la solidification des corps purs se fait à température constante , la chaleur libérée par la solidification (chaleur latente de fusion) compense la chaleur perdue par le refroidissement. Les transferts thermiques sont eux-mêmes modifiés par les changements de propriété de la matière associés au changement de phase.
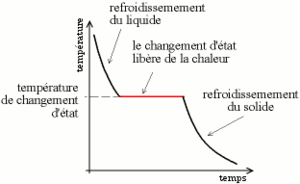
Courbe de solidification.
Dans le cas d'un mélange de corps purs, la température baisse en général au cours de la solidification (sauf dans le cas des eutectiques).
Surfusion
La courbe de refroidissement est en réalité légèrement différente. La température du liquide descend en dessous de la température de fusion, puis remonte brusquement pour former le plateau. Ceci s'appelle la surfusion.
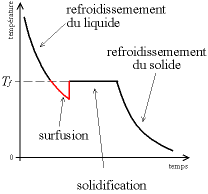
Courbe de surfusion.
La surfusion est due à l'énergie d'interface solide-liquide (tension superficielle). De manière simplifiée, on peut considérer que les petits germes de solide sont instables car ils sont dissous par l'agitation thermique, il faut attendre que le liquide soit « plus calme » pour qu'ils puissent se former. De manière plus rigoureuse, vu sous un angle thermodynamique, l'énergie libérée par la solidification (chaleur latente de fusion) ne compense pas l'énergie dépensée pour créer l'interface solide-liquide. Le liquide continue donc à se refroidir sans solidifier.
Lorsque le gain d'énergie est suffisant pour compenser la création de l'interface, les germes se créent très rapidement, et la chaleur libérée fait remonter la température. Puis, les germes croissent lentement, ce qui correspond au plateau.
Le gain d'énergie devient suffisant lorsque :
la température est suffisamment basse ;
une impureté vient diminuer l'énergie d'interface ; c'est le fameux exemple des chevaux du lac Ladoga rapporté par Malaparte (1942).
Bilan énergétique
Considérons un germe sphérique de rayon r. Il a un volume V de 4/3·π·r, ce qui correspond à la solidification d'une masse m = ρ·V si ρ est la masse volumique du solide. L'énergie EV libérée est donc, L désignant la chaleur latente de fusion EV = -L·m = -L·ρ·4/3·π·r.
Ce germe a une surface S = 4·π·r². Pour le créer, il faut donc dépenser une énergie ES qui vaut σ·S, où σ est la tension superficielle. On a donc ES = σ·4·π·r²
La création du germe n'est possible que si le système diminue son l'énergie, c'est-à-dire si EV + ES < 0 soit -L·ρ·4/3·π·r + σ·4·π·r² < 0 et donc si 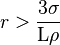
Comme σ diminue avec la température, les petits germes seront stables à basse température. Lorsque le système a juste la température de fusion, le rayon minimal est trop grand pour qu'un germe puisse se former. Ce rayon critique ne peut diminuer que si σ diminue, donc soit par l'arrivée d'une impureté, soit par la diminution de la température. L'impureté peut aussi se conduire comme un pré-germe de rayon suffisant.
Pour favoriser la solidification, on peut ainsi introduire un floculant (impureté), ou bien créer des défauts dans la paroi du récipient (par exemple des rayures ou des aspérités).
Solidification d'un système binaire
Solidification à l'équilibre
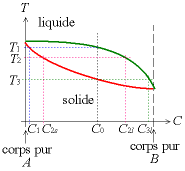
Diagramme binaire de solidification.
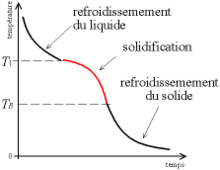
Courbe de solidification binaire.
Considérons un système binaire, c'est-à-dire un mélange de deux corps purs A et B. Le diagramme binaire de ce système permet de prédire la manière dont la solidification va se passer. Prenons pour simplifier le cas d'un système à solution solide unique.
Prenons un liquide composé de 100-C0 % de phase A et de C0 % de phase B (on utilise en général des concentrations massiques).
On suppose ici qu'à tout instant, tout le solide est à l'équilibre avec le liquide, ce qui signifie notamment que le solide est homogène. En pratique, cela signifie que la solidification est lente, et que la diffusion en phase solide permet d'homogénéiser le solide (la convection permet d'homogénéiser la phase liquide).
On met un liquide dans un moule, et on laisse le mélange refroidir. À la température T1 définie par l'intersection entre le liquidus et la droite verticale correspondant à C0, le premier germe solide se forme ; il se forme contre la paroi du récipient puisque c'est la partie la plus froide.
Ce premier germe est un solide à l'équilibre avec du liquide à T1 ; il se trouve donc sur le solidus, et a une concentration C1 ; on remarque que C1 vaut presque 0, c'est du corps A presque pur.
À une température donnée T2, la droite horizontale correspondant à cette température coupe le solidus à une concentration C2s et le liquidus à une concentration C2l. À cette température, le solide a une concentration 100-C2s de A ; le solide étant plus riche en A que le mélange initial, le liquide s'est appauvri et ne contient plus que 100-C2l % de A.
À la fin de la solidification, le solide a une teneur 100-C0 en A. Ceci détermine la température de fin de fusion T3. La dernière goutte de liquide à solidifier a une teneur 100-C3l en A, très faible, c'est presque du B pur ; comme le solide est encore légèrement plus riche en A que le mélange initial, cette goutte achève de « diluer » A.
Règle des leviers
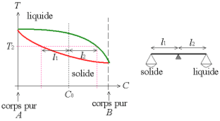
Diagramme binaire : la règle des moments.
Lorsque la solidification se fait à l'équilibre, le diagramme de phase permet de savoir quelle est la proportion de mélange qui a solidifié et quelle proportion reste liquide.
À une température T2 donnée, les cristaux formés ont une concentration C2s en A, et le liquide a une concentration C2l en A. La proportion de matière sous forme liquide et solide est donnée par la règle des leviers :
Règle des leviers — Considérons le segment horizontal T = T2 joignant le solidus et le liquidus ; ce segment est coupé par la droite verticale C = C0, ce qui forme deux segments de longueur l1 et l2 Le rapport des longueurs des segments l1/l2 ainsi définis donne le rapport des proportions de liquide et de solide.
C'est comme si l'on avait une balance dont le pivot n'est pas au centre du fléau, un des plateaux portant le liquide, l'autre le solide (d'où la référence au moment d'une force).
Solidification hors équilibre
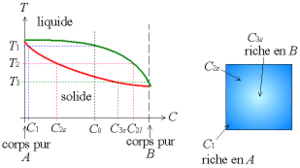
Diagramme binaire de solidification hors équilibre.
Maintenant, nous allons considérer que la solidification est trop rapide pour que la diffusion permette l'homogénéisation du solide. Alors, seule la couche superficielle du solide au contact avec le liquide est à l'équilibre ; la partie du solide sous cette couche superficielle est isolée du liquide et ne contribue donc pas à l'équilibre de solidification. C'est comme si la concentration C0 évoluait au cours de la solidification ; en effet, le liquide s'appauvrit en A et s'enrichit en B.
Comme précédemment, le premier germe est un solide à l'équilibre avec du liquide à T1 ; il se trouve donc sur le solidus, et a une concentration C1 ; on remarque que C1 vaut presque 0, c'est du corps A presque pur. Ces premiers germes se forment sur la paroi du moule (la partie la plus froide).
Le liquide s'appauvrit en A au fur et à mesure. À une température donnée T2, ce n'est pas le solide en entier qui a une concentration C2s, mais uniquement les germes formés à ce moment-là.
Le liquide continue à s'appauvrir au cours de la solidification, et les derniers germes formés, qui se trouvent au centre du moule, sont très riches en B pur ; la température de fin de fusion T3 est alors inférieure à la température de solidification à l'équilibre.
On voit que la pièce formée est hétérogène ; c'est la raison pour laquelle les glaçons ont des bulles au milieu (l'eau pure gèle sur les côtés et rejette l'air dissout vers le centre, jusqu'au moment où on a de l'air pur). Ce phénomène est appelé ségrégation.
Structure cristalline
Dans le cas où le solide formé est cristallin, la structure du lingot est en général la suivante :
tout au bord, on a une fine zone à structure équiaxe, appelée « peau » (chill zone) : les cristaux sont symétriques et isotropes (sans orientation préférentielle) ;
puis on a une structure colonnaire, également appelée « basaltique » : les cristaux sont allongés, perpendiculaires à la paroi, il y a une orientation cristalline préférentielle (texture) ;
dans certains cas, on observe des dendrites ;
au centre, une structure équiaxe : les cristaux sont symétriques et isotropes (sans orientation préférentielle).

 词典释义:
词典释义:
 ;
; ,
,
 ;
; ;
; ; 凝固; 凝
; 凝固; 凝