L'uranium est un élément chimique de symbole U et de numéro atomique 92, de la famille des actinides. C'est le 48 élément naturel du point de vue de l'abondance, son abondance est supérieure à celle de l'argent, comparable à celle du molybdène ou de l'arsenic, quatre fois moins abondant que le thorium. Il se trouve partout à l'état de traces, y compris dans l'eau de mer.
C'est un métal lourd radioactif (émetteur alpha) de période très longue (~ 4,4688 milliards d'années pour l'uranium 238 et ~ 703,8 millions pour l'uranium 235). Sa radioactivité, additionnée à celle de ses descendants dans sa chaîne de désintégration, développe une puissance de 0,082 watt par tonne d'uranium, ce qui en fait, avec le thorium 232 (quatre fois plus abondant, mais trois fois moins radioactif) et le potassium 40, la principale source de chaleur qui tend à maintenir les hautes températures du manteau terrestre, en ralentissant de beaucoup son refroidissement.
L'isotope U est le seul isotope fissile naturel. Sa fission libère une énergie voisine de 202,8 MeV par atome fissionné dont 9,6 MeV d'énergie non récupérable, communiquée aux neutrinos produits lors de la fission. L'énergie récupérable est plus d'un million de fois supérieure à celle des combustibles fossiles pour une masse équivalente. De ce fait, l'uranium est devenu la principale matière première utilisée par l'industrie nucléaire.
Pour son utilisation dans les réacteurs nucléaires, les réserves 3P (Prouvées + Probables + Possibles) d'uranium étaient estimées par l'AIEA à 5,4 millions de tonnes dans le monde en 2009 réparties essentiellement entre l'Australie (31 %), le Kazakhstan (12 %), le Canada (9 %) et la Russie (9 %) ; la production mondiale s'est élevée quant à elle à environ 50 000 tonnes en 2009 répartis entre le Kazakhstan (28 %), le Canada (20 %), l'Australie (16 %), la Namibie (9 %), la Russie (7 %), le Niger (6 %) et l'Ouzbékistan (5 %).
Uranium naturel
Le minerai d'uranium qui a été exploité par l'homme sur Terre possède une teneur en uranium pouvant varier de 0,1 % jusqu’à 20 %. L'uranium est dit naturel quand il est constitué d'isotopes dans leur proportion d'origine (identique pour tous les minerais d'uranium) : soit 99,2743 % d'uranium 238 accompagné de 0,7202 % d'uranium 235 et d'une quantité infime d'isotope 234 (0,0055%).
Découverte
L'uranite, ou pechblende, est le minerai d'uranium le plus commun.

Minerai d'uranium.
L'uranium fut mis en évidence en 1789 par le chimiste prussien Martin Heinrich Klaproth à partir de l'analyse d'un morceau de roche qu'on lui avait apporté de la mine de Saint Joachimsthal. Cette roche était de la pechblende, un minerai d'uranium qui contient principalement de l'U3O8. Klaproth parvint en la chauffant à en extraire un corps gris métallique. Dans sa communication du 24 septembre 1789 à l'Académie royale prussienne des sciences et intitulée « Ueber den Uranit, ein neues Halbmetall », il proposa le nom d'« urane » ou « uranite » au composé qu'il venait d'identifier (un oxyde d'uranium et non le corps pur), en référence à la découverte de la planète Uranus faite par William Herschel en 1781. Cet oxyde, rebaptisé uranium en 1790, avait comme propriété de donner une fine fluorescence aux verres et une couleur jaune verdâtre aux émaux, si bien que la pechblende était extraite de la mine de Joachimsthal et de mines d'étain en Cornouaille et des uranates alcalins utilisés (diuranate d'ammonium et de sodium) par les verriers de Bohême et les céramistes saxons.

Section polie de pechblende

Papier photographique impressionné par le rayonnement de la pechblende (reproduction de l'expérience de Becquerel)
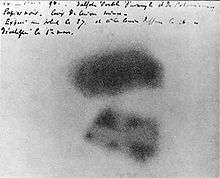
Papier photographique original irradié par le rayonnement de sel d'uranium (Expérience de Becquerel)
Ce n'est qu'en 1841 que le chimiste français Eugène-Melchior Péligot put l'isoler à l'état de pureté en réduisant le tétrachlorure d'uranium (UCl4) par le potassium. Il établit que l'urane était composé de deux atomes d'oxygène et d'un métal qu'il isola. L'uranium entra dans la nomenclature de la chimie. Il estima alors la masse volumique de l'uranium à 19 g/cm.
Le Français Henri Becquerel ne découvrit la radioactivité de l’uranium que beaucoup plus tard, le 28 février 1896, lorsqu'il constata que des plaques photographiques placées à côté de sels d'uranium (extraits d'un lot de pechblende de Joachimsthal) avaient été impressionnées sans avoir été exposées à la lumière. Les plaques avaient été noircies par les rayonnements émis par les sels : c'était la manifestation d'un phénomène jusqu'alors inconnu, la radioactivité naturelle. Pierre et Marie Curie isolèrent deux éléments nouveaux naturellement radioactifs, le polonium et le radium.
Gisements et exploitation
Le minerai d'uranium est appelé uraninite, ou pechblende. Les cinq plus gros producteurs au monde sont le Kazakhstan, le Canada, l'Australie, le Niger et la Namibie. À proximité des mines, l'uranium est concentré sous forme de yellowcake. Il est néanmoins trop peu concentré en isotope fissile pour être utilisé directement dans les centrales nucléaires de type Pressurized Water Reactor. C'est la raison pour laquelle il est souvent enrichi en uranium 235 par diffusion gazeuse ou centrifugation. Les centrales de type CANDU utilisent l'uranium non enrichi mais exigent beaucoup d'eau lourde comme modérateur.
Un Centre de recherche sur la géologie de l'uranium (Cregu) a été créé dans les années 1980, à Vandœuvre-lès-Nancy pour mieux connaitre la géologie et la géochimie de l'uranium et faciliter l'accès des prospecteurs à cette ressource, par exemple en le reliant aux discordances géologiques connues ou à découvrir
Abondance et répartition
L'uranium est répandu dans les profondeurs du globe terrestre. La désintégration d'uranium 238 et 235 et d'autres radionucléides comme le thorium 232 et ses descendants entretiennent encore en énergie thermique le noyau terrestre, mais surtout le manteau rocheux terrestre, et donc toute la géothermie.
Il est plus abondant dans la nature que l'or ou l'argent. Il est également présent dans toute l'écorce terrestre, surtout dans les terrains granitiques et sédimentaires, à des teneurs d'environ 2,7 g/tonne (soit donc 2,7 ppm). Ainsi, le sous-sol d'un jardin sur un carré de 20 m de côté peut-il en contenir, sur une profondeur de 10 m, environ 24 kg, ce qui fait de l'ordre du millier de milliards de tonnes rien que pour l'écorce terrestre, sans compter le manteau. En termes de réserve mondiale, cependant, l'immense majorité de cette masse est bien sûr inexploitable dans les conditions économiques actuelles. La teneur du minerai varie beaucoup selon les roches, de 0,1 ppm dans les carbonates à 350 ppm dans les phosphates.
L'eau de mer contient environ 3,3 mg d'uranium par mètre cube selon le CEA et la COGEMA, soit 4,5 milliards de tonnes d'uranium dissous dans les océans.
Les eaux douces en contiennent souvent aussi en diverses concentrations. La concentration moyenne du Rhône en uranium est de 0,5 μg/L. La masse d’uranium transitant chaque jour dans le Rhône peut ainsi être estimée à environ 80 kg, soit près de trente tonnes par an, provenant essentiellement du ruissellement des roches uranifères des Alpes. Pourtant, en extraire de l'eau ne serait pas énergétiquement rentable.
On estime à 5,5 millions de tonnes l'uranium extractible à US59 $ par livre , et 35 million de tonnes sont classées comme ressources minérales éventuellement économiques à extraire .
La production industrielle a commencé après 1945 pour atteindre 10 000 t/an. dès 1953, 50 000 t. en 1958, décroit jusqu'à 30 000 t en 1965, remonte jusqu’à un plateau de 65 000 en 1980, redescend jusqu’à 30 000 t. dans les années 1990 et remonte dans les années 2000.
En 2009, la production mondiale était estimée à 50 572 tonnes, dont 27,3 % extraites du Kazakhstan qui a connu une forte hausse de production dans les années 2000 passant de 3 300 t en 2001 à 17 803 t en 2003. Cette hausse s'est poursuivie en faisant le leader mondial avec 33 % (soit 17 803 tonnes en 2010) et d'importantes réserves minières (17 % de la réserve mondiale). Selon l'OCDE, l'intensification de la production de ce pays a permis une augmentation de plus de 25 % de la production mondiale de 2008 à 2010.
D'autres ressources importantes sont détenues par le Canada (20,1 %), l'Australie (15,7 %), la Namibie (9,1 %), la Russie (7,0 %), et le Niger (6,4 %). De nouvelles ressources ont été trouvées, mais avec des coûts d'extraction et/ou raffinage augmentés.
L'uranium est une ressource non renouvelable (comme tous les métaux), non recyclable, et pas toujours facilement exploitable dans des conditions socialement, économiquement et/ou écologiquement acceptables. Les réserves facilement accessibles sont en cours d'épuisement, mais il reste des réserves plus coûteusement accessibles pour au moins un siècle selon l'OCDE et qui seront épuisées dans moins d'un siècle, selon les experts du Energy Watch Group (en). La quantité d'énergie extractible à partir de l'uranium naturel pourrait théoriquement être multipliée (jusqu'à 40 fois) grâce à la surgénération et au retraitement qui permettraient de fissionner la majeure partie des atomes d'uranium initialement extrait de la mine.
Dans l'eau de mer et les eaux naturelles
Les concentrations en uranium (l'élément chimique uranium) dans les eaux « naturelles » sont les suivantes :
L'eau de mer : 3,3 µg/L
Le Rhône : 0,56 µg/L (débit annuel d’uranium = 29 tonnes)
L'Indus : 4,94 µg/L
Le Gange : 7 µg/L
Le fleuve Jaune : 7,5 µg/L
Dans les eaux de boisson :
Eau de Badoit : 58 µg/L à la source, 5,45 µg/L après traitement
Eau de Vichy : 20 µg/L.
Le seuil OMS pour les eaux de boisson était fixé jusqu'en 2011 à 15 µg/L, puis en 2011 la quatrième édition des "Directives pour la qualité de l'eau de boisson" l'a fixé à 30 µg/l.
Cinétique hydrogéologique
La solubilité de l’uranium est liée aux conditions d’oxydoréduction du milieu. Dans des conditions oxydantes (augmentation de la concentration en oxygène dissous), l’uranium devient plus facilement soluble (passage de la valence IV à la valence VI). Les conditions oxydantes favorisent la complexation de l’uranium en solution avec certains ligands. Les principaux ligands sont, par ordre d’affinité décroissante:
les carbonates,
les groupements hydroxyles,
les nitrates,
les phosphates.
L’uranium présente une très forte affinité pour les oxyhydroxydes de fer. Cette adsorption peut s’effectuer très rapidement lors de changements des conditions d’oxydoréduction, une diminution de la teneur en oxygène (condition réductrice) engendre une précipitation rapide de l’uranium sous formes d’oxyde (UO2). C'est une telle précipitation qui est par exemple à l'origine du gisement d'Oklo.
Synthèse chimique des fluorures d'uranium (UFx)
Deux étapes sont nécessaires à la synthèse :
le raffinage : Le minerai d'uranium pulvérisé « yellowcake » — est dissous dans l'acide nitrique, fournissant une solution de nitrate d'uranyle UO2(NO3)2. éventuellement filtration. Le nitrate d'uranyle pur est obtenu par extraction par solvant, avec une solution de TBP.
Le minerai d'uranium pulvérisé « yellowcake » — est dissous dans l'acide nitrique, fournissant une solution de nitrate d'uranyle UO2(NO3)2.
éventuellement filtration.
Le nitrate d'uranyle pur est obtenu par extraction par solvant, avec une solution de TBP.
Cette étape permet d'obtenir un nitrate d'uranyle UO2(NO3)2 de grande pureté (>99,95 %).
la conversion en elle-même : précipitation du nitrate d'uranyle par l'ammoniac gazeux pour obtenir du diuranate d'ammonium (NH4)2U2O7 (DUA), calcination du diuranate d'ammonium, vers 400 °C, pour produire l'UO3, réduction de l'UO3 par l'hydrogène pour obtenir de l'UO2, hydrofluoration d'UO2 par l'acide fluorhydrique HF dans un four pour produire du tétrafluorure d'uranium UF4, réduction de l'UF4 avec du calcium finalement pour obtenir du métal pur.
précipitation du nitrate d'uranyle par l'ammoniac gazeux pour obtenir du diuranate d'ammonium (NH4)2U2O7 (DUA),
calcination du diuranate d'ammonium, vers 400 °C, pour produire l'UO3,
réduction de l'UO3 par l'hydrogène pour obtenir de l'UO2,
hydrofluoration d'UO2 par l'acide fluorhydrique HF dans un four pour produire du tétrafluorure d'uranium UF4,
réduction de l'UF4 avec du calcium finalement pour obtenir du métal pur.
Yellowcake + nitrate d'uranyle
+ Diuranate
+ Dioxyde d'uranium
+ UF4
Propriétés
Propriétés radiologiques
Produit fissile naturel
L'uranium 235 est le seul nucléide naturel qui soit fissile (ou, très rarement, fissible), autrement dit il peut, par capture de neutron, se scinder en deux noyaux fils avec émission de neutrons (fission nucléaire). Par suite, l'uranium enrichi en cet isotope est aujourd'hui utilisé comme combustible nucléaire dans les réacteurs nucléaires (voir cycle du combustible nucléaire) ou encore dans les armes nucléaires, que ce soient les bombes atomiques, ou comme amorce dans les bombes H.
Au contraire de l'uranium 235, l'uranium 238, lorsqu'il capture un neutron, ne fissionne pas (sauf neutrons rapides). Il devient de l'uranium 239 instable qui, par désintégration β, va se transformer en neptunium 239. Or ce dernier est lui aussi radioactif β, et va alors donner naissance à un nouveau noyau, le plutonium 239. Ce radioisotope est fissile, comme l'uranium 235. L'uranium 238 est un isotope fertile, qui peut produire des produits fissiles.
L'uranium 234 n'est, lui, ni fissile, ni fertile, et provient de la décomposition radioactive de l'uranium 238 comme indiqué dans la précédente section.
La fission d'un atome d'uranium 235 libère de l'ordre de 193,2 MeV d'énergie récupérable en réacteur (la valeur exacte dépendant des produits de fission) et 9,6 MeV communiquée aux neutrinos inutiles et quasiment indétectables. De même, la fission d'un atome de plutonium 239 libère de l'ordre de 198,6 MeV d'énergie récupérable et 8,6 MeV communiquée aux neutrinos. Ces valeurs sont à comparer avec celles de la combustion de carburants fossiles, qui libèrent de l'ordre de 5 eV par molécule de CO2 produit: l'ordre de grandeur des énergies libérées par les combustibles nucléaires est un million de fois plus importante que celle des énergies fossiles chimiques.
Le potentiel d'énergie de l'uranium n'est exploité que très partiellement dans les réacteurs actuels, mais la différence reste nette : 1 kg d'uranium naturel permet la production d'environ 500 000 MJ dans un réacteur conventionnel, à comparer avec les 49 MJ obtenus par 1 kg de gaz naturel, 45 MJ pour 1 kg de pétrole, et 20 à 30 MJ pour le charbon.
Les isotopes de l'uranium naturel
L'uranium possède 26 isotopes connus, tous radioactifs, dont 3 seulement sont présents à l'état naturel : U ; U et U. On trouve dans une tonne d'uranium naturel pur 7,2 kg d'uranium 235 et 56 g d'uranium 234, le reste étant de l'uranium 238.
-
Uranium 238 et uranium 235
Les isotopes U et U ont beaucoup d'applications, militaires notamment, mais aussi civiles, comme la datation de l'âge de la Terre à partir de la datation radiométrique par l'uranium-plomb ou par l'uranium-thorium.
Quelles que soient les teneurs en uranium des milieux, les proportions entre les deux principaux isotopes formant l'uranium naturel sont pratiquement les mêmes : U : 99,28 % ; U : 0,72% ; U : 0,0056 %.
La proportion d'U décroît à l'échelle des temps géologiques. Leur rapport de formation dans une supernova est de un à 1,65, c'était (approximativement) la proportion de l'uranium présent sur Terre il y a ~4,5 milliards d'années, ce qui est juste inférieur à l'âge de la formation de ces isotopes (voir formation et évolution du système solaire). Il y a deux milliards d'années, lors de la période de fonctionnement du réacteur nucléaire naturel d'Oklo, la proportion d'U était encore de près de 4 %, ce qui a permis à ce gisement d'atteindre la criticité, lors de la précipitation des composés dissous formant le nouveau minerai.
-
Uranium 234
Le troisième isotope, U, appartient à la chaîne de désintégration de l'U. L'isotope 234 est toujours présent sur Terre, à l'état de traces, bien qu'il ait une demi-vie de seulement 245 500 ans ; car il est constamment créé par désintégration radioactive de l'isotope 238 (après 3 étapes : une transition α donnant Th, puis deux transitions β donnant Pa, puis U). Quand il est à l'équilibre séculaire, la proportion entre U et U est égale au rapport des demi-vies, soit 0,0056 %.
Cependant, les rapports isotopiques peuvent varier légèrement d'un gisement à l'autre, entre 0,005 % et 0,006 % pour l'U, du fait d'une légère différence de comportement dans le changement U↔ U . Le rapport isotopique U/U peut être perturbé par différents processus environnementaux, tandis que le rapport U/U reste assez largement constant.
-
Autres isotopes
L'industrie nucléaire produit deux autres isotopes artificiels de l'uranium, relativement stables à échelle humaine :
L'isotope 236 est produit en réacteur par irradiation de l'isotope 235, qui dans près de 18 % des cas ne fissionne pas mais absorbe un neutron. Il tend à s'accumuler dans l'uranium de recyclage, dont il augmente fortement la radioactivité, et dont (étant neutrophage) il diminue le potentiel énergétique. Bien qu'ayant une demi-vie de 23 millions d'années, presque du centuple de celle de l'isotope 234, cet isotope a disparu depuis longtemps dans la nature. Son produit est du thorium 232, qui s'est « confondu » avec le thorium 232 « initial » et se trouve à présent majoritairement sous cette forme ainsi que des éléments de sa chaîne de désintégration.
L'isotope 233 est un élément fissile produit en réacteur par irradiation du thorium. Il est à la base du cycle du thorium. Sa demi-vie de 159 000 ans est largement supérieure à celle du plutonium.
Activité massique
Spectre gamma d'un minerai d'uranium, permet d'identifier la présence des radionucléides Ra, Pb, Bi de la chaîne de désintégration de l'uranium 238 (lui-même non émetteur gamma).
L'uranium pur est radioactif, son activité massique dépendant à la fois de son enrichissement, et de la fraîcheur de sa purification chimique.
Si l'on considère les isotopes purs de l'uranium, U a une activité massique de 12,4 Bq/mg, U de 80 Bq/mg, et U de 230 Bq/µg, soit 230 000 Bq/mg — quatre ordres de grandeur au-dessus des précédents.
L'uranium naturel, quand il est chimiquement purifié (essentiellement composé de U et de U en équilibre avec son descendant U), a une activité spécifique de l'ordre de 25 Bq/mg. En amont, à poids égal d'uranium, la radioactivité d'un minerai, où il est en équilibre avec tous les éléments radioactifs de sa chaîne de désintégration, est naturellement 3 (si le Radon peut s'échapper) à 7 fois plus importante.
L'uranium enrichi est plus actif, partiellement du fait de l'activité plus importante de U (6,33 fois plus radioactif que l'U), mais surtout à cause de la concentration différentielle en U (10 000 fois plus radioactif que U), toujours présent à l'état de traces dans la chaîne de désintégration de l'isotope 238. Elle atteint typiquement 2 500 Bq/mg pour un enrichissement de 90 % (uranium dit de qualité militaire). Pour les enrichissements de l'ordre de 3 %, destinés aux centrales nucléaires, l'activité spécifique est de l'ordre de 60 Bq/mg.
Inversement, l'uranium appauvri est presque entièrement débarrassé non seulement de sa fraction de l'isotope 235, mais également de son descendant l'isotope 234. Immédiatement après l'enrichissement, son activité massique tend à se rapprocher de celle de U pur, c'est-à-dire de l'ordre de 12,5 Bq/mg (en pratique, un peu plus du fait de la présence résiduelle d'U). Cependant, l'équilibre entre U et ses deux premiers descendants (le thorium 234 de période 24 jours, et le protactinium 234) est atteint rapidement, en 2 mois. La radioactivité spécifique à l'équilibre (avec ses deux premiers descendants) étant déjà de 41,5 Bq/mg.
Sections efficaces
Aux neutrons thermiques, avec:
σa= Section efficace d'absorption (= capture + fission le cas échéant)
σf= Section efficace de fission
À 20 °C
U: σa = 585,9 barns ; σf = 532,8 barns
U: σa = 676,1 barns ; σf = 568,4 barns
U: σa = 2,72 barns
À 240 °C
U: σa = 587,3 barns ; σf = 534,9 barns
U: σa = **7,0 barns ; σf = 543,1 barns
U: σa = 2,60 barns
À 300 °C
U: σa = 588,9 barns ; σf = 536,1barns
U: σa = **2,4 barns ; σf = 538,8 barns
U: σa = 2,58 barns
Propriétés chimiques

Valences
III (rouge),
IV (vert),
V (instable) et
VI (jaune) de l'uranium
De symbole U, l'uranium est le dernier élément naturel du tableau périodique. Chaque atome d'uranium possède 92 protons et entre 125 et 150 neutrons.
À l'état pur, l'uranium solide est un métal radioactif gris à blanc (voire argenté), qui rappelle la couleur du nickel. Il est dur et très dense. De plus, l'uranium est l'atome le plus lourd (qui contient le plus de nucléons) présent naturellement sur la Terre.
En raison de son affinité pour l'oxygène, l'uranium s'enflamme spontanément dans l'air à température élevée, voire à température ambiante lorsqu'il se trouve sous forme de microparticules. Il est pyrophorique.
L’uranium a quatre valences possibles (+III à +VI), les valences IV et VI étant les plus répandues dans les minerais. Les conditions de passage de la valence IV à la valence VI dépendent du potentiel d’oxydoréduction du milieu.
Ainsi dans la nature, l'élément uranium se retrouve toujours combiné à d’autres éléments, tels l'oxygène, l'azote, le soufre, le carbone sous forme d'oxydes, de nitrates, de sulfates ou de carbonates. On le trouve, par exemple, combiné à l'oxygène dans l'uranite et la pechblende, deux des principaux minerais d'uranium, constitués d'oxyde uraneux (UO2).
Enfin, les ions uranyle UO2 se dissolvent très bien dans la plupart des acides, comme dans l'acide nitrique HNO3 ou l'acide fluorhydrique HF en donnant des sels d'uranyle tels que le nitrate d'uranyle UO2(NO3)2. L'équation de la dissolution de l'ion uranyle en sel d'uranyle dans l'acide nitrique est la suivante :
UO2 + 2 NO3 → UO2(NO3)2.
Dérivé organo-uranien
Comme la plupart des métaux, l'uranium a une chimie organo-métallique et de nombreux complexes organo-métalliques tel l'uranocène sont connus.
Applications
Utilisations historiques
Plateau en ouraline fluorescent sous éclairage ultraviolet.
Le minerai d'uranium a été utilisé comme pigment dans la verrerie, la céramique et la faïence, sous forme de diuranate de sodium ou d'ammonium. Dans le verre, l'uranium est typiquement utilisé à des concentrations de 0,1 % à 2 % en masse pour produire de l'ouraline, solide d'un jaune fluorescent ou légèrement vert facile à identifier. Il a été utilisé pour colorer des céramiques dentaires à de très faibles concentrations. Il produit une pigmentation jaune à faibles concentrations, puis crème, orange, brune, verte, ou noire, quand la concentration augmente.
Il sert également de catalyseur dans certaines réactions chimiques spécialisées et dans des films photographiques.
L'uranium appauvri a également été utilisé pour ces emplois physico-chimiques. Sous forme d'acétate d'uranyle et de zinc (réactif de Blanchetière), il donne des cristaux jaune-vert fluorescents avec les ions sodium Na+. Il permet donc de caractériser facilement ce métal lors des analyses en chimie minérale.
Industrie nucléaire

Pastilles de combustible nucléaire d'uranium.
Historiquement, la première utilisation du minerai d'uranium par l'industrie nucléaire a été d'en extraire le radium, pour des applications médicales.
Le principal usage contemporain de l'uranium exploite ses propriétés nucléaires.
L'uranium 235 est le seul isotope fissile naturel, ce qui permet l'exploitation de l'uranium dans les réacteurs nucléaires (après un éventuel enrichissement), ainsi que pour la fabrication d'armes nucléaires (après un fort enrichissement).
L'uranium 238 est à la fois fissible dans les réacteurs à neutrons rapides, et fertile : par capture neutronique il se transforme finalement en plutonium 239, fissile. Il est envisagé d'exploiter cette double possibilité dans le cycle du combustible nucléaire, pour des cycles fondés sur la combustion du plutonium.
L'uranium 233, qui peut être artificiellement produit par irradiation du thorium, est également fissile en neutrons thermiques. Cette possibilité est à la base d'un cycle surgénérateur fondé sur le thorium.
Contrôle des matières nucléaires
L'uranium est une matière nucléaire dont la détention est réglementée (Article R1333-1 du code de la défense).
Uranium appauvri
L'uranium appauvri, un sous-produit de l'enrichissement de l'uranium, est très prisé pour sa dureté et sa densité. Il est pyrophorique, employé comme arme antichar dotée d'un fort pouvoir à la fois pénétrant et incendiaire : à très haute vitesse, il perfore aisément les blindages en s'enflammant lors de l'impact, provoquant un incendie qui fait exploser le véhicule touché. Ainsi, des munitions à base d'uranium appauvri (obus de 20 à 30 mm des avions ou hélicoptères chasseurs de chars) ont été utilisées lors des guerres du Golfe (guerre du Koweït et guerre en Irak) et du Kosovo.
Dans ses emplois militaires, l'uranium appauvri est également utilisé pour faire des plaques de blindages.
L'uranium appauvri a aussi été utilisé comme contrepoids en aviation, sur les premiers Boeing 747, les McDonnell Douglas DC-10, les Lockheed L-1011 TriStar par exemple, ce qui pose le problème du recyclage de ces avions qui, pour beaucoup, arrivent en fin de vie. Dans cet emploi, il est progressivement remplacé par le tungstène. La quille de certains voiliers de compétition a contenu de l'uranium appauvri avant que la réglementation n'interdise son usage.
Il est également plus efficace que le plomb pour les écrans de protection radiologique.
Avec un complément de plutonium, l'uranium appauvri constitue un combustible nucléaire appelé « combustible MOX ». Il sert d'élément fertile dans les réacteurs, où l'U se transforme par irradiation en Pu fissile.
Toxicité
Toxicité chimique
L'uranium présente une toxicité comparable à celle d'autres métaux lourds, du même ordre que celle du plomb. La dose létale pour l'homme semble être de quelques grammes.
La majeure partie de l’uranium pénétrant dans l’organisme (plus de 95 %) n’est pas absorbée et s’élimine dans les fèces. Environ 67 % de l’uranium sanguin est filtré par les reins et excrété dans les urines dans les 24 heures.
Le système digestif absorbe globalement entre 0,2 et 2 % de l’uranium présent dans l’eau et les aliments. Les composés solubles de ce métal sont plus facilement absorbés que les composés insolubles. Le contenu normal d'un corps humain en équilibre avec son environnement est de l'ordre de 90 à 150 µg d'uranium, résultant d'un apport journalier de l'ordre de 1 à 2 µg/jour par l'eau courante et l'alimentation. Les deux tiers s'accumulent dans les os, 16 % dans le foie, 8 % dans les reins et 10 % dans les autres tissus.
Le rein est l'organe critique pour la toxicité chimique. Les études à long terme portant sur des professionnels exposés à l’uranium ont signalé certains troubles de la fonction rénale selon l’intensité de l’exposition. Il semblerait néanmoins d’après certaines données que ces troubles puissent être transitoires et que la fonction rénale revienne à la normale après élimination de la source d’une exposition excessive. Le seuil de toxicité chimique rénale est estimé à 70 µg/kg de poids corporel ou 16 µg/g de rein (limite de 3 µg/g de rein pour la protection des travailleurs).
Radiotoxicité
Contrairement à la radioactivité, qui se mesure en becquerels, la radiotoxicité de l'uranium (c'est-à-dire l'effet de son rayonnement ionisant sur l'homme) se mesure en μSv (microsievert).
Quel que soit son enrichissement, la radioactivité de l'uranium est toujours du type alpha de l'ordre de 4,5 MeV. Sa radiotoxicité dépend donc de son activité massique et faiblement de sa composition. Elle est de l'ordre de 0,6 µSv/Bq (F) à 7 µSv/Bq (S) en inhalation, 0,05 µSv/Bq (F) à 0,008 µSv/Bq (S) en ingestion, les poumons et les os étant alors les organes critiques.
La radiotoxicité de l'uranium serait du même ordre de grandeur que celle de la toxicité chimique : elle l'emporte pour des enrichissements supérieurs à 6 %, la toxicité chimique étant sinon prépondérante.
Effets sur la reproduction
L'uranium est aussi reprotoxique via notamment un effet délétère sur les organes reproducteurs ; soit du fait de sa radioactivité, soit du fait de sa chimiotoxicité, et peut-être des deux. L'uranium a chez l'animal des effets démontrés ; sur le système reproducteur: Chez le rongeur de laboratoire, la barrière hémato-testiculaire (ou BHT) qui était réputée protéger le testicule peut en être franchie par le plutonium, l'américium et le polonium au moins grâce à la transferrine.
De l'uranium est significativement trouvé dans les testicules de rats ayant reçu un implant d'uranium dans le muscle d'une des pattes. Les récepteurs à la transferrine présent dans l'épithélium séminifère humain pourrait donc expliquer la présence d'uranium dans le sperme de soldats blessés par des munitions à l'uranium appauvri.
Des rats ayant des implants sous-cutanés d'uranium, et des souris abreuvées d'eau contenant de l'uranium produisent des cellules de Leydig altérées, ce qui perturbe la production d'hormones stéroïdes et se traduit par un sperme dégradé (spermatozoïdes moins nombreux et moins mobiles), expliquant les observations faites dès 1949 de diminution du nombre de portées et du nombre de petits par portée chez plusieurs espèces d'animaux ayant régulièrement ingéré de faibles doses de nitrate d'uranyle.
Effets sur le développement
il induit une toxicité fœtale et embryonnaire chez la souris chez laquelle un implant d'uranium a été posé dans le muscle d'une patte.
il est tératogène à doses plus élevées, avec mort de l'embryon exposé à une concentration 50 mg·kg·j durant 9 jours, 20 % inférieure à la dose létale pour l'adulte.
une souris gestante abreuvée avec une eau correspondant à une ingestion de 25 mg d'uranium/kg/j produit moins de jeunes. Ceux-ci ont ensuite des problèmes de développement et de survie.
La plupart des études et réglementations se fondent sur les effets sur l'animal, or les premières études ex vivo permises par les nouvelles techniques de cultures cellulaires laissent penser que les gonades humaines seraient plus sensibles à l'uranium que ne le sont celles des rongeurs utilisés en laboratoire. Le testicule fœtal humain pourrait aussi être plus sensible que ceux des rongeurs de labo.
Normes
Il n'y a pas de consensus sur les normes ni la NOAEL (dose sans effet nocif observé) de l'uranium, certains estimant que les effets délétères de la radioactivité peuvent exister quelle que soit la dose.
Pour la potabilité de l'eau, l'OMS a fixé une teneur maximale de 1,4 mg·l, tout en recommandant dans ses lignes directrices une concentration en uranium cent fois plus faible, inférieure à 15 µg/l, pour les eaux de boisson courante.
Prix
![Prix « spot » mensuel de l'uranium en US$[58].](https://wiki-gateway.eudic.net/wikipedia_fr/I/m/MonthlyUraniumSpot.png)
Prix « spot » mensuel de l'uranium en US$.
Le prix de l'uranium a baissé dans les années 1980 et 1990 pour plusieurs raisons :
les politiques d'économie d'énergie ont permis de limiter la consommation d'électricité ;
des gisements d'uranium économiquement exploitable ont été découverts ;
les stocks d'uranium militaire constitués dans le contexte de la guerre froide ont été convertis en stocks civils et utilisés dans les réacteurs nucléaires à la suite de l'assouplissement des tensions américano-soviétiques.
Le prix de l'uranium a atteint un minimum en janvier 2001 à 6,40 $ par livre de U3O8.
Le prix de l'uranium a progressivement augmenté depuis 2001 pour atteindre un pic à 135 $ en juin 2007. Ce pic s'explique par la diminution des stocks, la faible augmentation de production, et par des événements ponctuels tels que l'inondation de la mine de Cigar Lake au Canada et l'incendie de la mine Olympic Dam en Australie.
L'uranium est redescendu à 46,50 $ en août 2010. En janvier 2011, il se situait à environ 63 $. Il est à prévoir une tendance à la hausse en raison de l'épuisement des stocks militaires prévu vers 2015.
Le prix de revient du kWh est peu sensible au prix de l’uranium. Certes, le coût du cycle du combustible représente environ 20 % du prix de revient du kWh, mais ce cycle comprend toutes les transformations physiques et chimiques qu’il faut faire subir à l’uranium naturel pour en faire un combustible utilisable. En conséquence, le prix du minerai d’uranium ne dépasse guère 7 % du coût total du kWh. Cependant, des études économiques montrent que le prix de l'uranium commence à avoir un effet significatif sur le coût du kWh d'électricité nucléaire à partir de 50 ou 100 € par livre de U3O8.
Commerce
La France importe plus que la consommation d'uranium qui lui est nécessaire et exporte ses surplus sous différentes formes, d'après les douanes françaises. En 2014, le prix moyen à la tonne à l'export était de 36 000 €.

 词典释义:
词典释义:
 ;
; ;
; ,易燃
,易燃 ;
; ;
;






![Prix « spot » mensuel de l'uranium en US$[58].](https://wiki-gateway.eudic.net/wikipedia_fr/I/m/MonthlyUraniumSpot.png)
